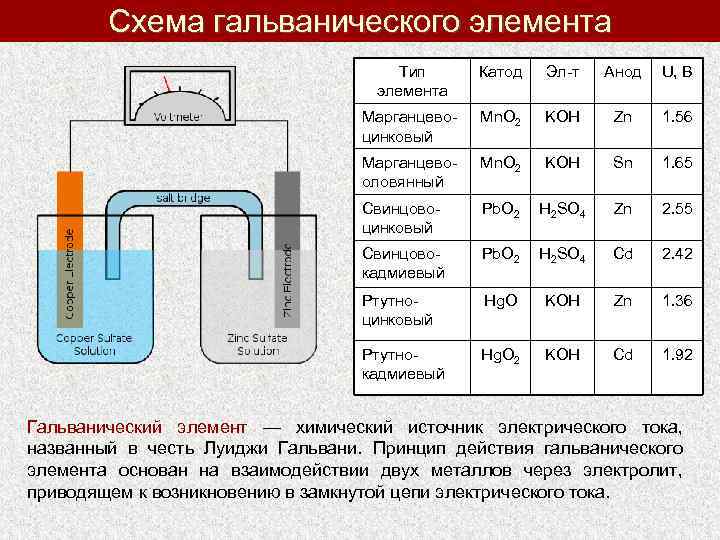
Изготовление батарейки
При изготовлении демонстрационной батареи гальванических элементов будем использовать стандартную пару – медь и цинк. Медную фольгу можно найти в некоторых трансформаторах. В крайнем случае, можно сделать медный электрод из свернутой в спираль голой медной проволоки . Цинк можно добыть из разрядившихся солевых элементов питания, как правило, в них остается достаточно много металлического цинка даже, когда элемент непригоден к дальнейшему использованию. Вместо раствора кислоты, возьмем 10% раствор поваренной соли. В качестве емкости для электролита взяты пластиковые емкости от витаминов объемом примерно 50-100 мл.

В качестве контактов использованы винты, которые одновременно закрепляю электроды на крышке. При этом крайне желательно крепить медные электроды латунным винтом. Цинковую пластину можно без проблем крепить стальным винтом. Для герметизации под гайку подложена подходящая по размеру резиновая сантехническая прокладка.

Батарея из трех гальванических элементов позволяет питать светодиод.

Напряжение на одном элементе батареи составляет около 1 В.

Ток, отдаваемый в нагрузку, составляет около 0,23 мА

Такого тока достаточно для свечения светодиода. Однако на фотографии это свечение можно заметить, только если снимать при большой светочувствительности.

Такую батарею можно использовать в школе, например для выполнения лабораторной работы, по определению внутреннего сопротивления источника тока .
Как работает сухая батарейка (солевой гальванический элемент)
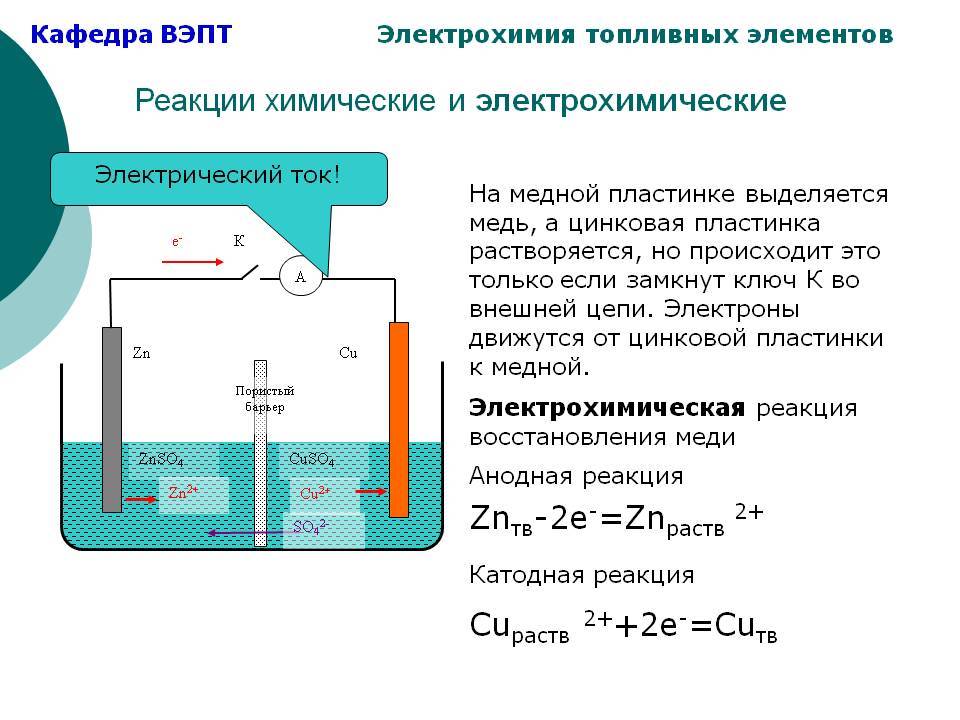
Рассмотрим процессы, происходящие в сухом элементе. При потреблении тока электроны поступают через внешнюю электрическую цепь с цинкового электрода на угольный стержень. Происходят следующие реакции:
- Анод: Zn → Zn 2+ + 2e−.
- На угольном стержне электроны расходуются на восстановление H3O+ — ионов. Катод: 2H3O+ + 2e− → H2 + 2H2O.
- Ионы H3O+ образуются в результате частичного протолиза NH4+ — ионов электролита: NH4+ + H2O H3O+ + NH3.
- При восстановлении H3O+ — ионов образуется водород, который не может удалиться (корпус герметичен) и образует вокруг угольного стержня прослойку газа (поляризация угольного электрода). Ток медленно затухает. Чтобы избежать образования водорода, угольный электрод окружают слоем диоксида марганца (MnO2). В присутствии диоксида марганца H3O+ — ионы восстанавливаются с образованием воды. 2MnO2 + 2H3O+ + 2e− → 2MnO (OH) + 2H2O. Таким способом избегают поляризации электрода, а диоксид марганца называют деполяризатором. Электролит NH4Cl диссоциирует и частично протолизируется.
- В общем: 2NH4Cl + 2H2O 2NH3 + 2H3O+ + 2Cl−.
- Образующиеся на аноде ионы Zn2+ поступают в раствор и образуют труднорастворимую соль Zn2+ + 2NH3 + 2Cl− → Cl2.
- Анод: Zn — 2e− → Zn2+.
- Катод: 2MnO2 + 2H3O+ + 2e− → 2MnO (OH) + 2H2O.
- Раствор электролита: Zn2+ + 2NH4+ + 2Cl− + 2H2O Cl2 + 2H3O+.
- Общая реакция: Zn + 2MnO2 + 2NH4Cl → 2MnO (OH) + Cl2.
Способ второй: банка с электролитом
Для сборки своими руками устройства, похожего по конструкции на первую батарейку в мире, понадобится стеклянная банка или стакан. Для материала электродов используем цинк или алюминий (анод) и медь (катод). Для увеличения эффективности элемента их площадь должна быть максимально большой. Провода лучше будет припаять, но к электроду из алюминия провод придется прикрепить заклепкой или болтовым соединением, так как паять его сложно.
Электроды погружаются внутрь банки так, чтобы они не соприкасались друг с другом, и концы их находились выше уровня банки. Лучше их зафиксировать, установив распорку или крышку с прорезями. Для электролита используем водный раствор нашатыря (50 г на 100 мл воды). Водный раствор аммиака (нашатырный спирт) – это не тот нашатырь, который используется для нашего опыта. Нашатырь (хлористый аммоний) – это порошок без запаха белого цвета, применяющийся при пайке в качестве флюса или как удобрение.
https://youtube.com/watch?v=yeWnPoQ3cSY
Второй вариант приготовления электролита – сделать 20% раствор серной кислоты. При этом нужно заливать кислоту в воду, и ни в коем случае не наоборот. Иначе вода мгновенно закипит и ее брызги вместе с кислотой попадут на одежду, лицо и глаза.
Осталось налить получившийся раствор в банку так, чтобы до краев сосуда оставалось не менее 2 мм свободного пространства. Затем при помощи тестера подобрать необходимое количество банок.
Собранный своими руками элемент питания похож по составу на солевую батарейку, так как содержит хлорид аммония и цинк.
ГАЛЬВАНИЧЕСКИЕ ЭЛЕМЕНТЫ: САМОДЕЛЬНАЯ БАТАРЕЯ
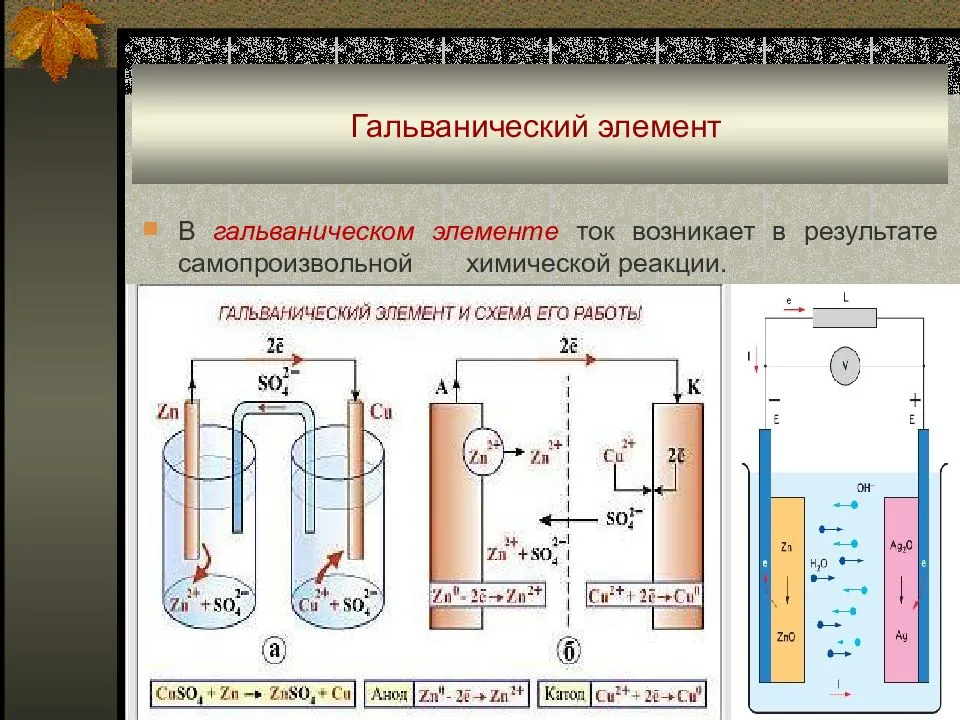
Каждому из нас знакомы химические источники тока различных типов и форм. Но как это часто случается, мы редко задумываемся о том, как устроен этот совершенно привычный и обыденный предмет. А между тем, появление первых химических источников тока, положило начало превращению электричества из лабораторной диковинки в нашего повседневного помощника.
Правильное объяснение этому явлению смог дать другой итальянский ученый Алессандро Вольта. Он установил, что это явление связано с наличием двух разнородных металлов, соприкасающихся с электролитом, в роли которого выступала кровь лягушки, а сама лапка играла лишь роль чувствительного индикатора электрического тока . Опираясь на свои исследования Вольта в 1799г. создал первый химический источник тока. В этом устройстве Вольта использовал медный и цинковый электроды, погруженные в раствор серной кислоты.

Цинк бурно реагирует с кислотами. В раствор переходят не атомы цинка, а положительные ионы, так что в электроде остается избыток электронов, следовательно, цинковая пластина заряжается отрицательно. Вообще, большинство металлов при погружении в электролит заряжается отрицательно, на поверхности медной пластинки протекает подобный процесс. Но избыток отрицательных зарядов на медном электроде гораздо меньше, а значит, относительно цинкового электрода его потенциал получается более высоким. Если соединить внешним проводником медную и цинковую пластины, то электроны начнут перемещаться с цинковой пластины на медную, т.е. в цепи потечет электрический ток .
Часто напряжения, даваемого одним гальваническим элементом, недостаточно. Тогда их можно соединять последовательно в батареи.

Вообще изготовить химический источник тока совсем нетрудно: надо поместить в электролит две пластинки из разных металлов . Такие гальванические элементы возникают самопроизвольно. Например, намочил дождь крышу, покрытую оцинкованным железом, на железе наверняка имеются царапины, так, что и железо, и цинк вступили в контакт с водой, которая играет роль электролита. Цинк в такой паре начнёт активно разрушаться, а вот железо не пострадает, пока не разрушится весь цинк. Именно для этого и покрывают железо слоем цинка.
Нагляднее всего можно пронаблюдать гальваническую коррозию на примере контактов железа с цинком и медью в растворе соли. Железные скрепки были надеты на цинковую и медную пластины и погружены в раствор соли.

Через сутки скрепка, соединенная с медной пластиной, покрылась ржавчиной. В то время, как скрепка, бывшая в контакте с цинком, совершенно не пострадала.

Ученые составили электрохимический ряд напряжений металлов. Чем дальше друг от друга отстоят металлы в этом ряду, тем более высокое напряжение дает гальванический элемент, составленный из этих металлов. Так пара золото – литий теоретически может дать электродвижущую силу (ЭДС) 4,72 В. Но такая пара в водной среде работать не сможет – литий это щелочной металл, легко реагирующий с водой, а золото стоит слишком дорого для подобного применения.
На практике элемент Вольта обладает рядом серьёзных недостатков.
- Во-первых, электролитом ему служит весьма едкая жидкость – раствор серной кислоты. Жидкий электролит всегда представляет собой неудобство или даже опасность. Он может расплескаться, разлиться при повреждении корпуса.
- Во-вторых, на медном электроде такого элемента будет выделяться водород. Это явление называется поляризацией. По многим свойствам водород весьма близок к металлам, так что его пузырьки создадут дополнительную ЭДС поляризации, стремящейся вызвать ток противоположного направления . Кроме того, пузырьки газа не пропускают электрический ток, что тоже ведет к ослаблению тока. Поэтому приходится периодически встряхивать сосуд, удаляя пузырьки механически, или вводя в состав электролита специальные деполяризаторы.
- В третьих, в процессе работы гальванического элемента Вольта, цинковый электрод постепенно растворяется. Теоретически, когда гальванический элемент не используют, разрушение цинкового электрода должно прекратиться, но поскольку почти всегда в составе цинка есть примеси других металлов, они при соприкосновении с электролитом играют роль второго электрода, образуя короткозамкнутый элемент, что ведет к гальванической коррозии цинкового электрода . Для того, чтобы устранить этот недостаток, приходится использовать сверхчистый цинк или конструктивно предусматривать возможность извлечения цинкового электрода из электролита. Так что когда батарея не используется, электролит из нее следует сливать.
Но для демонстрационных целей всеми этими недостатками можно пренебречь, если заменить серную кислоту более безопасным электролитом.
Напряжение ячейки
Напряжение (электродвижущая сила Eо), производимый гальваническим элементом, можно оценить по стандартной Свободная энергия Гиббса изменение электрохимической реакции согласно
Eклеткао=−Δрграммо(νеF){ displaystyle E _ { text {cell}} ^ {o} = – Delta _ {r} G ^ {o} / ( nu _ {e} F)}
куда νе – количество электронов, перенесенных в уравновешенных полуреакциях, и F является Постоянная Фарадея. Однако его можно определить более удобно, используя стандартная таблица потенциалов для двоих полуклетки участвует. Первый шаг – идентифицировать два металла и их ионы, взаимодействующие в клетке. Затем каждый смотрит вверх стандартный электродный потенциал,Eо, в вольт, для каждого из двух половина реакции. Стандартный потенциал ячейки равен более положительному Eо значение минус более отрицательное Eо ценить.
Например, на рисунке выше растворы CuSO4 и ZnSO4. В каждом растворе есть соответствующая металлическая полоска и солевой мостик или пористый диск, соединяющий два раствора и позволяющий ТАК2−4 ионы свободно перемещаются между растворами меди и цинка. Чтобы вычислить стандартный потенциал, ищем полуреакции меди и цинка и находят:
- Cu2+ + 2 е− ⇌ Cu Eо = +0,34 В
- Zn2+ + 2 е− ⇌ Zn Eо = −0,76 В
Таким образом, общая реакция такова:
- Cu2+ + Zn ⇌ Cu + Zn2+
Стандартный потенциал для реакции равен +0,34 В – (-0,76 В) = 1,10 В. Полярность ячейки определяется следующим образом. Металлический цинк восстанавливает сильнее, чем металлическая медь, потому что стандартный (восстановительный) потенциал цинка более отрицательный, чем у меди. Таким образом, металлический цинк теряет электроны на ионы меди и развивает положительный электрический заряд. В константа равновесия, K, для ячейки задается
- перK=νеFEклеткаорТ{ displaystyle ln K = { frac { nu _ {e} FE _ { text {cell}} ^ {o}} {RT}}}
куда F это Постоянная Фарадея, р это газовая постоянная и Т это температура в кельвины. Для ячейки Даниэля K примерно равно 1.5×1037. Таким образом, в состоянии равновесия переносится несколько электронов, достаточное для зарядки электродов.
Фактические потенциалы полуэлементов должны быть рассчитаны с использованием Уравнение Нернста поскольку растворенные вещества вряд ли будут в своем стандартном состоянии,
- Eполуклетка=Eо−рТνеFпереQ{ displaystyle E _ { text {half-cell}} = E ^ {o} – { frac {RT} { nu _ {e} F}} ln _ {e} Q}
куда Q это коэффициент реакции. Когда заряды ионов в реакции равны, это упрощается до
- Eполуклетка=Eо−2.303рТνеFбревно10{Mп+}{ displaystyle E _ { text {half-cell}} = E ^ {o} -2,303 { frac {RT} { nu _ {e} F}} log _ {10} left {{ text {M}} ^ {n +} right }}
где {Mп+} это Мероприятия иона металла в растворе. На практике вместо активности используется концентрация в моль / л. Металлический электрод находится в стандартном состоянии, поэтому по определению имеет единичную активность. Потенциал всей клетки получается как разность потенциалов двух полуэлементов, поэтому он зависит от концентраций обоих растворенных ионов металла. Если концентрации одинаковы, Eклетка=Eклеткао{ displaystyle E _ { text {cell}} = E _ { text {cell}} ^ {o}}и уравнение Нернста не требуется в предполагаемых здесь условиях.
Стоимость 2.303рF является 1.9845×10−4 В / К, поэтому при 25 ° C (298,15 K) потенциал полуячейки изменится всего на 0,05918 В /νе если концентрация иона металла увеличивается или уменьшается в 10 раз.
- Eполуклетка=Eо−0.05918 Vνебревно10Mп+{ displaystyle E _ { text {half-cell}} = E ^ {o} – { frac {0.05918 { text {V}}} { nu _ {e}}} log _ {10} слева }
Эти расчеты основаны на предположении, что все химические реакции находятся в равновесии. Когда в цепи протекает ток, условия равновесия не достигаются, и напряжение ячейки обычно снижается с помощью различных механизмов, таких как развитие перенапряжения. Кроме того, поскольку химические реакции происходят, когда ячейка вырабатывает электроэнергию, концентрация электролита изменяется, а напряжение ячейки снижается. Следствием температурной зависимости стандартных потенциалов является то, что напряжение, создаваемое гальваническим элементом, также зависит от температуры.
Самодельный простой гальванический элемент. Зарядка мобильного телефона без электросети. | ДелайСам.Ру

Те, кто на даче не имеют электричества, наверняка испытывают определенные неудобства в самых элементарных вещах. Ну ладно там, нет холодильника или телевизора… Но ведь порой даже мобильный телефон подзарядить нет возможности. Запасных аккумуляторов — не напасешься и не навозишься.
Между тем, существует довольно простой способ получить электрический ток достаточный для работы простейших электронных устройств прямо на месте и без больших затрат.
Да, лампочку к такому источнику не подключить, но обеспечить электропитанием небольшой радиоприемник или подзарядить мобильник ему вполне по силам. Такой же источник сможет зарядить небольшие аккумуляторы и в походе, пока туристы спят или отдыхают.
И что особенно ценно, данный источник стоит буквально копейки, работает независимо ни от каких погодных условий и не имеет вообще никаких подвижных частей.
Принцип работы данного источника тока основан на том, что некоторые металлы образуют между собой т.н. гальванические пары. Т.е.
при их соприкосновении образуется простейший гальванический элемент, вырабатывающий электрический ток. Например, по этой причине нельзя соединять напрямую провода из меди и алюминия.
Если два электрода из таких металлов поместить в электролит, они начнут вырабатывать электрический ток. Почему же не использовать этот эффект для того, что бы решить хотя бы одну проблему — с той же зарядкой мобильного телефона в условиях отсутствия электросети.
При устройстве такого простейшего элемента можно использовать в качестве электродов любые медные и железные отрезки проволоки, а лучше — пластины. Пластины дадут бОльший ток. А качестве электролита подойдет сырая земля (грунт), которую лучше пропитать солевым раствором.
Что бы не портить землю на своем участке, лучше насыпать землю в ведра (можно и дырявые) или даже в полиэтиленовые пакеты.
Разумеется, напряжение такого элемента невелико — 0,5-1 вольт максимум. А ток, который он вырабатывает 20-50 мА. Но что нам мешает сделать несколько таких элементов и соединить их последовательно! Таким образом мы достигнем необходимого напряжения, достаточного для зарядки аккумулятора мобильного телефона или другого устройства.
Разумеется, такой элемент примитивен, имеет невысокий КПД. Но! Во-первых, он крайне дешев и делается действительно из материалов, которые валяются под ногами — (проволока, обрезки труб, пластины металла).
Во-вторых, он не требует никаких телодвижений с вашей стороны после его изготовления. Он необслуживаемый! Один раз сделал — пользуйся весь сезон. Ну разве что поливай периодически, поддерживая влажности грунта.
В третьих — сделать его по силам даже школьнику младших классов.
Такими элементами пользовались еще на заре электроники, когда батареи были очень дефицитны и дороги. Теперь же с появлением весьма экономичных и низковольтных электронных приборов массового пользования они возможно кому то снова смогут принести пользу.
К. Тимошенко
Половина реакции и условности
В полуячейке металл пополам состояния окисления. Внутри изолированной полуячейки находится Снижение окисления (окислительно-восстановительная) реакция, которая находится в химическое равновесие, условие, символически записанное следующим образом (здесь “M” представляет катион металла, атом, который имеет дисбаланс заряда из-за потери “п«электроны):
- Mп+ (окисленные виды) + пе− ⇌ M (редуцированные виды)
Гальванический элемент состоит из двух полуэлементов, так что электрод одного полуэлемента состоит из металла A, а электрод другого полуэлемента состоит из металла B; Таким образом, окислительно-восстановительные реакции для двух отдельных полуэлементов:
- Ап+ + пе− ⇌ А
- Bм+ + ме− ⇌ B
Общая сбалансированная реакция
- м А + п Bм+ ⇌ п B + м Ап+
Другими словами, атомы металла одной полуячейки окисляются, а катионы металлов другой полуячейки восстанавливаются. Разделив металлы на две полуячейки, их реакцией можно управлять таким образом, чтобы обеспечить перенос электронов через внешнюю цепь, где они могут быть полезными. работай.
Электроды соединяются металлической проволокой по порядку проводить электроны, участвующие в реакции.
- В одной полуячейке растворенные катионы металла-B объединяются со свободными электронами, которые доступны на границе раздела между раствором и электродом металла-B; эти катионы тем самым нейтрализуются, заставляя их осадок из раствора в виде отложений на электроде металла-B, процесс, известный как покрытие.
- Эта реакция восстановления заставляет свободные электроны по всему электроду металла-B, проволоке и электроду металла-A втягиваться в электрод металла-B. Следовательно, электроны отталкиваются от некоторых атомов электрода металла-A, как если бы катионы металла-B реагировали с ними напрямую; эти атомы металла-A становятся катионами, которые растворяются в окружающем растворе.
- По мере продолжения этой реакции в полуячейке с электродом металла-A образуется положительно заряженный раствор (потому что в нем растворяются катионы металла-A), в то время как в другой полуячейке образуется отрицательно заряженный раствор (поскольку катионы металла-B выпадать из него в осадок, оставляя после себя анионы); неослабевая, этот дисбаланс в ответственности остановит реакцию. Растворы полуэлементов соединены солевым мостиком или пористой пластиной, которая позволяет ионам переходить от одного раствора к другому, что уравновешивает заряды растворов и позволяет реакции продолжаться.
По определению:
- В анод – электрод, на котором происходит окисление (потеря электронов) (электрод металл-А); в гальваническом элементе это отрицательный электрод, потому что при окислении электроны остаются на электроде. Эти электроны затем проходят через внешнюю цепь к катоду (положительный электрод) (в то время как при электролизе электрический ток движет поток электронов в противоположном направлении, а анод является положительным электродом).
- В катод – электрод, на котором происходит восстановление (усиление электронов) (электрод металл-В); в гальваническом элементе это положительный электрод, так как ионы восстанавливаются, забирая электроны с электрода и снимая пластину (в то время как при электролизе катод является отрицательной клеммой и притягивает положительные ионы из раствора). В обоих случаях утверждение КотХод привлекает Котions ‘верно.
Гальванические элементы по своей природе производят постоянный ток. В Клетка Вестона имеет анод, состоящий из кадмий Меркурий амальгама, и катод из чистой ртути. Электролит представляет собой (насыщенный) раствор сульфат кадмия. В деполяризатор представляет собой пасту сульфата ртути. Когда раствор электролита насыщен, напряжение ячейки очень воспроизводимо; следовательно, в 1911 году он был принят как международный стандарт напряжения.
Батарея – это набор гальванических элементов, которые соединены вместе и образуют единый источник напряжения. Например, типичный 12В свинцово-кислотная батарея имеет шесть подключенных гальванических ячеек последовательно с анодами из свинца и катодами из диоксида свинца, оба погружены в серную кислоту. Большой аккумуляторные, например, в обмен телефонами Обеспечивая питание телефонов пользователей центрального офиса, ячейки могут быть подключены как последовательно, так и параллельно.
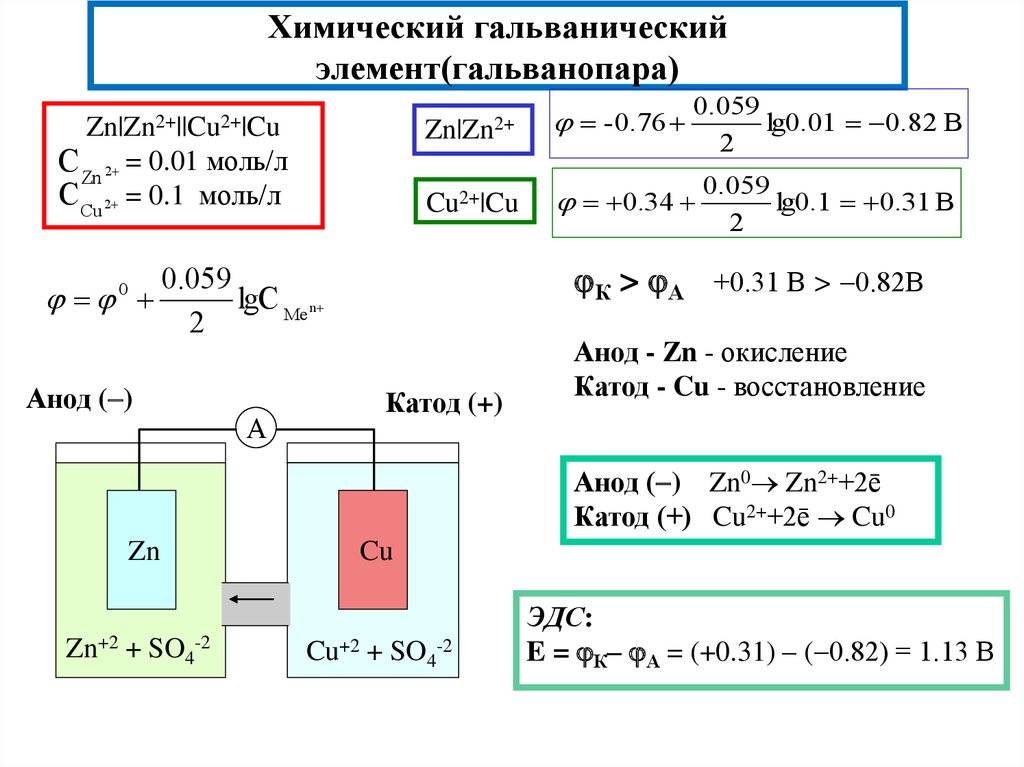
Как устроен гальванический элемент Даниэля-Якоби, или Так где же все-таки электрический ток?
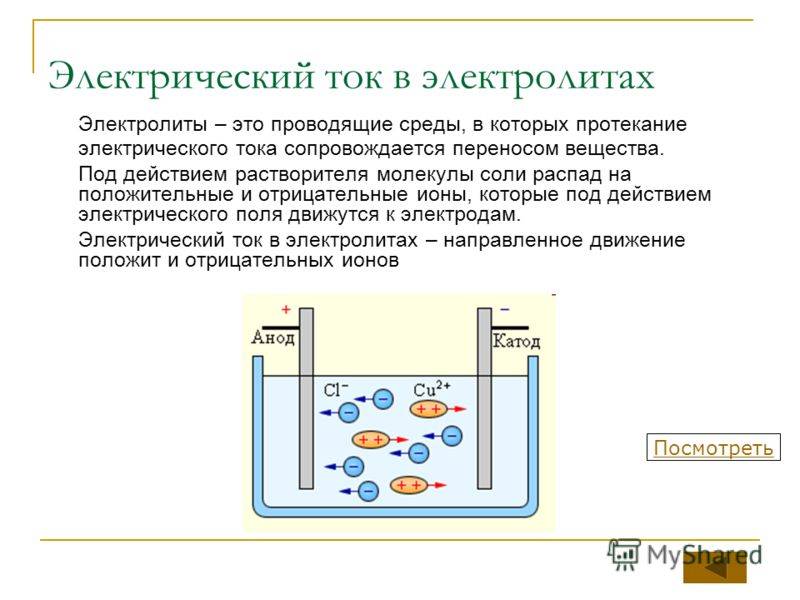
Известно, что электрический ток – это направленное движение заряженных частиц (электронов).
На активном металле скапливаются электроны, а поверхность малоактивного металла, заряжается положительно. Если соединить проводником (например, металлической проволокой) оба металла, то электроны с одного перейдут на другой, а двойной электрический слой перестанет существовать. Это будет означать возникновение электрического тока.
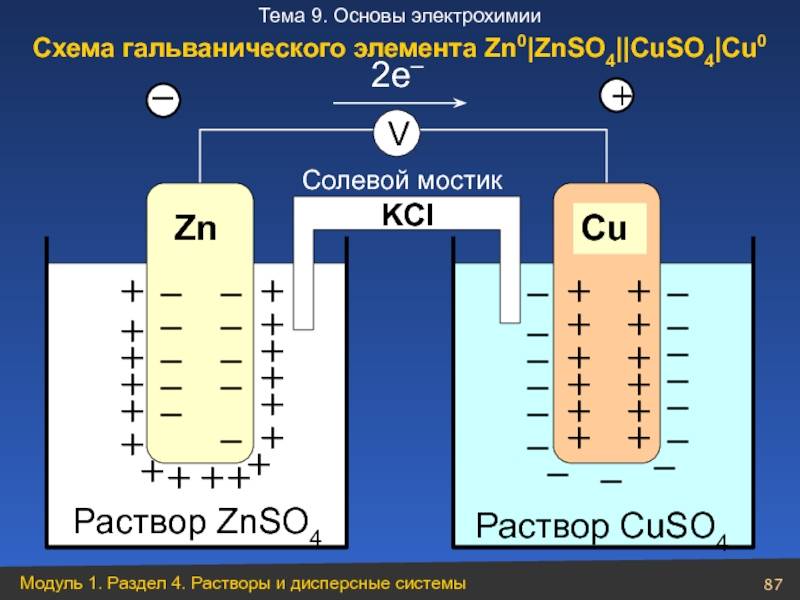
Причем, ток возникает за счет окислительно-восстановительного процесса: активный металл окисляется (так как отдает электроны малоактивному), а малоактивный металл восстанавливается (так как принимает электроны от активного). Металлы друг с другом не соприкасаются, а взаимодействуют через посредника: внешнего проводника. Данная схема и есть схема гальванического элемента. Именно так устроен и работает гальванический элемент Даниэля-Якоби:
В схеме элемента показан «солевой мостик». Он представляет собой трубку, в которой присутствует электролит, не способный взаимодействовать ни с , ни с электролитами в пространствах у электродов. Например, это может быть раствор сульфата натрия Na2SO4. Подобный мостик нужен для того, чтобы уравновешивать (нейтрализовать) заряды, образующиеся в растворах гальванического элемента.
Таким образом, возникшая электрическая цепь замыкается: анод → проводник с гальванометром → катод → раствор в катодном пространстве → «солевой мостик» → раствор в анодном пространстве → анод.
– электрод, на котором происходит окисление (цинковая пластинка):

Электроны цинка Zn отправляются по внешней цепи (то есть по проводнику) на катод.
– электрод, на котором происходит восстановление (медная пластинка):

Катионы меди Cu2+, пришедшие на пластинку из раствора сульфата меди (II), получают электроны цинкового анода.
В общем виде весь процесс окисления-восстановления в гальваническом элементе выглядит так:

Для любого гальванического элемента можно составить запись в виде схемы. Например, для приведенного элемента Даниэля-Якоби она будет выглядеть так:

Здесь:
1 – анод;
2 – катод;
3 – скачок потенциала (граница раздела фаз);
4 – электролит в анодном пространстве;
5 – электролит в катодном пространстве;
6 – граница между растворами (солевой мостик).
Или сокращенно:
Нормативные документы
Учитывая большое количество электроэлементов, для их буквенно-цифровых (далее БО) и условно графических обозначений (УГО) был разработан ряд нормативных документов исключающих разночтение. Ниже представлена таблица, в которой представлены основные стандарты.
Таблица 1. Нормативы графического обозначения отдельных элементов в монтажных и принципиальных электрических схемах.
Читать также: Виды рукояток для ножей
| Номер ГОСТа | Краткое описание |
| 2.710 81 | В данном документе собраны требования ГОСТа к БО различных типов электроэлементов, включая электроприборы. |
| 2.747 68 | Требования к размерам отображения элементов в графическом виде. |
| 21.614 88 | Принятые нормы для планов электрооборудования и проводки. |
| 2.755 87 | Отображение на схемах коммутационных устройств и контактных соединений |
| 2.756 76 | Нормы для воспринимающих частей электромеханического оборудования. |
| 2.709 89 | Настоящий стандарт регулирует нормы, в соответствии с которыми на схемах обозначаются контактные соединения и провода. |
| 21.404 85 | Схематические обозначения для оборудования, используемого в системах автоматизации |
Следует учитывать, что элементная база со временем меняется, соответственно вносятся изменения и в нормативные документы, правда это процесс более инертен. Приведем простой пример, УЗО и дифавтоматы широко эксплуатируются в России уже более десятка лет, но единого стандарта по нормам ГОСТ 2.755-87 для этих устройств до сих пор нет, в отличие от автоматических выключателей. Вполне возможно, в ближайшее время это вопрос будет урегулирован. Чтобы быть в курсе подобных нововведений, профессионалы отслеживают изменения в нормативных документах, любителям это делать не обязательно, достаточно знать расшифровку основных обозначений.
Устройство и принцип работы гальванического элемента

Металл, погруженный в раствор электролита, называется электродом.
Электроды — это система двух токопроводящих тел — проводников первого и второго рода.
К проводникам первого рода относятся металлы, сплавы, оксиды с металлической проводимостью, а также неметаллические материалы, в частности графит; носители заряда — электроны.
К проводникам второго рода относятся расплавы и растворы электролитов; носители заряда — ионы.
Устройство, состоящее из двух электродов, называется гальваническим элементом.
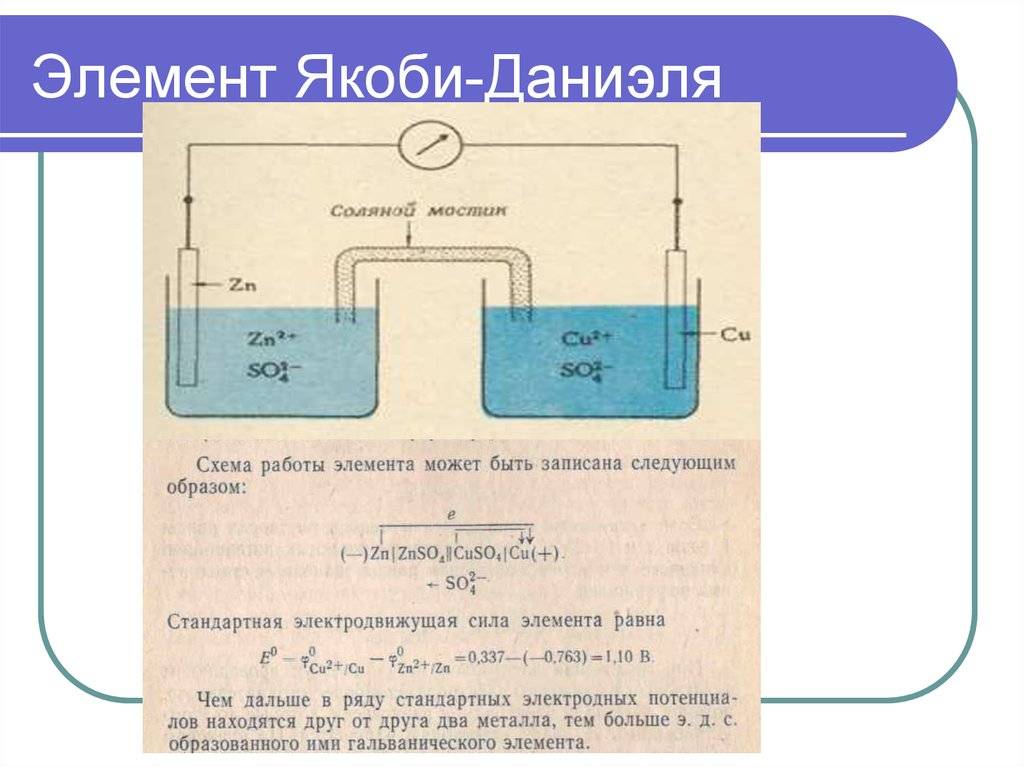
| Рис. 2. Схема медно-цинкового гальванического элемента |
Рассмотрим гальванический элемент Якоби—Даниэля (схема приведена на рис. 2). Он состоит из цинковой пластины, погруженной в раствор сульфата цинка, и медной пластины, погруженной в раствор сульфата меди. Для предотвращения прямого взаимодействия окислителя и восстановителя электроды отделены друг от друга пористой перегородкой.
В гальваническом элементе электрод, сделанный из более активного металла, т.е. металла, расположенного левее в ряду напряжений, называют анодом, а электрод, сделанный из менее активного металла — катодом.
На поверхности цинкового электрода (анода) возникает двойной электрический слой и устанавливается равновесие:
Zn0 – 2ē ←→ Zn2+.
В результате протекания этого процесса возникает электродный потенциал цинка.
На поверхности медного электрода (катода) также возникает двойной электрический слой и устанавливается равновесие:
Cu2+ + 2ē ←→ Cu0.
В результате возникает электродный потенциал меди.
Так как потенциал цинкового электрода имеет более отрицательное значение, чем потенциал медного электрода, то при замыкании внешней цепи, т.е. при соединении цинка с медью металлическим проводником, электроны будут переходить от цинка к меди. В результате этого процесса равновесие на цинковом электроде смещается вправо, поэтому в раствор перейдет дополнительное количество ионов цинка. В то же время равновесие на медном электроде сместится влево и произойдет разряд ионов меди.
Таким образом, при замыкании внешней цепи возникают самопроизвольные процессы растворения цинка на цинковом электроде и выделения меди на медном электроде. Данные процессы будут продолжаться до тех пор, пока не выровняются потенциалы или не растворится весь цинк или не высадится на медном электроде вся медь.
Итак, при работе гальванического элемента Якоби—Даниэля протекают следующие процессы:
1. Анодный процесс, процесс окисления:
Zn0 – 2ē → Zn2+.
2. Катодный процесс, процесс восстановления:
Cu2+ + 2ē → Cu0.
3. Движение электронов во внешней цепи.
4. Движение ионов в растворе: анионов SO42– к аноду, катионов Cu2+ к катоду. Движение ионов в растворе замыкает электрическую цепь гальванического элемента.
Суммируя электродные реакции, получим:
Zn + Cu2+ = Zn2+ + Cu.
В результате протекании данной реакции в гальваническом элементе возникает движение электронов во внешней цепи и ионов внутри элемента, т.е. электрический ток. Поэтому суммарную химическую реакцию, протекающую в гальваническом элементе, называют токообразующей реакцией.
Электрический ток в гальваническом элементе возникает за счет окислительно-восстановительной реакции, протекающей так, что окислительные и восстановительные процессы оказываются пространственно разделенными: на отрицательном электроде (аноде) происходит процесс окисления, на положительном электроде (катоде) — процесс восстановления.
Необходимым условием работы гальванического элемента является разность потенциалов электродов. Максимальная разность потенциалов электродов, которая может быть получена при работе гальванического элемента, называется электродвижущей силой (ЭДС) элемента. Она равна разности между потенциалом катода и потенциалом анода элемента:
ЭДС = Eк – Ea . (1)
ЭДС элемента считается положительной, если токообразующая реакция в данном направлении протекает самопроизвольно. Положительной ЭДС отвечает и определенный порядок в записи схемы элемента: записанный слева электрод должен быть отрицательным. Например, схема элемента Якоби—Даниэля записывается в виде:
Zn │ ZnSO4 ║ CuSO4 │ Cu .
Разновидности гальванических элементов
Самыми распространенными считают угольно-цинковые элементы. В них применяется пассивный угольный коллектор тока, контактирующий с анодом, в качестве которого выступает оксид марганца (4). Электролитом является хлорид аммония, применяемый в пастообразном виде.
Он не растекается, поэтому сам гальванический элемент называют сухим. Его особенностью является возможность «восстанавливаться» на протяжении работы, что позитивно отражается на продолжительности их эксплуатационного периода. Такие гальванические элементы имеют невысокую стоимость, но невысокую мощность. При понижении температуры они снижают свою эффективность, а при ее повышении происходит постепенное высыхание электролита.
Щелочные элементы предполагают использование раствора щелочи, поэтому имеют довольно много областей применения.
В литиевых элементах в качестве анода выступает активный металл, что позитивно отражается на сроке эксплуатации. Литий имеет отрицательный электродный потенциал, поэтому при небольших габаритах подобные элементы имеют максимальное номинальное напряжение. Среди недостатков подобных систем можно выделить высокую цену. Вскрытие литиевых источников тока является взрывоопасным.
Об этой статье
wikiHow работает по принципу вики, а это значит, что многие наши статьи написаны несколькими авторами. При создании этой статьи над ее редактированием и улучшением работали, в том числе анонимно, 29 человек(а). Количество просмотров этой статьи: 21 845.
Категории: Дом и сад
English:Make a Homemade Battery
Español:hacer una batería casera
Português:Fazer Uma Pilha Caseira
Italiano:Costruire una Batteria fatta in Casa
Deutsch:Eine Batterie selber bauen
Français:fabriquer soi‐même une pile
Bahasa Indonesia:Membuat Baterai Rumahan
العربية:صنع بطارية منزلية الصنع
Nederlands:Zelf een batterij maken
한국어:집에서 건전지 만드는 방법
日本語:自家製電池を作る
Печать
Литиевая батарейка
Литий-марганцевая диоксид батарейка -это относительно недавняя разработка, использующая преимущества высокого электродного потенциала и плотности энергии металлического лития. Она предлагает значительно большую плотность энергии и емкость, чем “щелочная” и угольная, при относительно небольшом увеличении стоимости.
Литий находится в форме очень тонкой фольги и запрессован внутри банки из нержавеющей стали, чтобы сформировать отрицательный электрод.
Положительный электрод – диоксид марганца, смешанный с углеродом для улучшения его проводимости, а электролит-перхлорат лития растворен в пропиленкарбонате.
Номинальное напряжение на клеммах литиевого элемента составляет 3,0 в, что в два раза больше, чем у “щелочных” и других гальванических элементов. Он также имеет очень низкую скорость саморазряда, что дает ему очень длительный срок хранения. Внутреннее сопротивление также довольно низкое и остается таким в течение всего срока службы.
Литиевая батарея хорошо работает при низких температурах, даже ниже -60 °C, и передовые разработки используют их в спутниках связи, космических аппаратах, военных и медицинских приложениях. Медицинские приложения, требующие длительного срока службы критически важных устройств, таких как искусственные кардиостимуляторы и другие имплантируемые электронные медицинские устройства, используют специализированные литий-ионные батареи, которые могут работать в течение многих лет.
Литиевые гальванические элементы батарейки подходят для менее важных применений для работы с игрушками, часами и камерами. Хотя литиевые батареи стоят дороже, они обеспечивают более длительный срок службы, чем “щелочные” батареи, и сводят к минимуму их замену.
На практике, однако, напряжение на клеммах уменьшается по мере уменьшения заряда. Именно по этой причине, в отличие от вторичных батарей, первичные, как правило, не получают спецификации емкости ни в ампер-часах, ни в миллиампер-часах от большинства производителей вместо этого обычно задается только максимальный ток разряда.
Литиевые гальванические элементы обладают значительно большей плотностью энергии и емкостью, чем “щелочные” и другие первичные батареи; они обеспечивают более высокое (примерно в два раза) напряжение на клеммах по сравнению с другими первичными элементами, и напряжение на клеммах остается почти постоянным в течение всего срока службы.
Рекомендации
- Кейтли, Джозеф Ф (1999). Дэниэл Селл. Джон Уайли и сыновья. С. 49–51. ISBN 978-0-7803-1193-0.
- Оствальд, Вильгельм (1980). Электрохимия: история и теория.
- Хотон, Брайан (2007) Скрытая история: потерянные цивилизации, тайные знания и древние тайны. Карьера Пресса. ISBN . стр. 129–132
- Ashcroft, N.W .; Мермин, Н. Д. (1976). Физика твердого тела. Форт-Уэрт, Техас: Харкорт.
- ^
- Аткинс, П; де Паула (2006). Физическая химия. J. (8-е изд.). Издательство Оксфордского университета. ISBN 978-0-19-870072-2. Глава 7, разделы «Равновесная электрохимия»
- Аткинс, П; де Паула (2006). Физическая химия. J. (8-е изд.). Издательство Оксфордского университета. ISBN 978-0-19-870072-2. Раздел 25.12 «Рабочие гальванические элементы»
Способ первый: батарейка из лимона
Эта самодельная батарейка будет использовать электролит на основе лимонной кислоты, содержащаяся в мякоти лимона. Для электродов возьмем медную и железную проволочки, гвозди или булавки. Положительным будет медный электрод, а отрицательным – железный.
Лимон нужно разрезать поперек на две части. Для большей устойчивости половинки кладутся в небольшие емкости (стаканы или рюмки). Необходимо присоединить провода к электродам и погрузить их в лимон на расстоянии 0,5 – 1 см.
Теперь нужно взять мультиметр и измерить напряжение на получившемся гальваническом элементе. Если его недостаточно, то потребуется еще изготовить своими руками несколько одинаковых лимонных батареек и соединить их последовательно с помощью тех же проводов.