§ 35. Электрический ток в электролитах
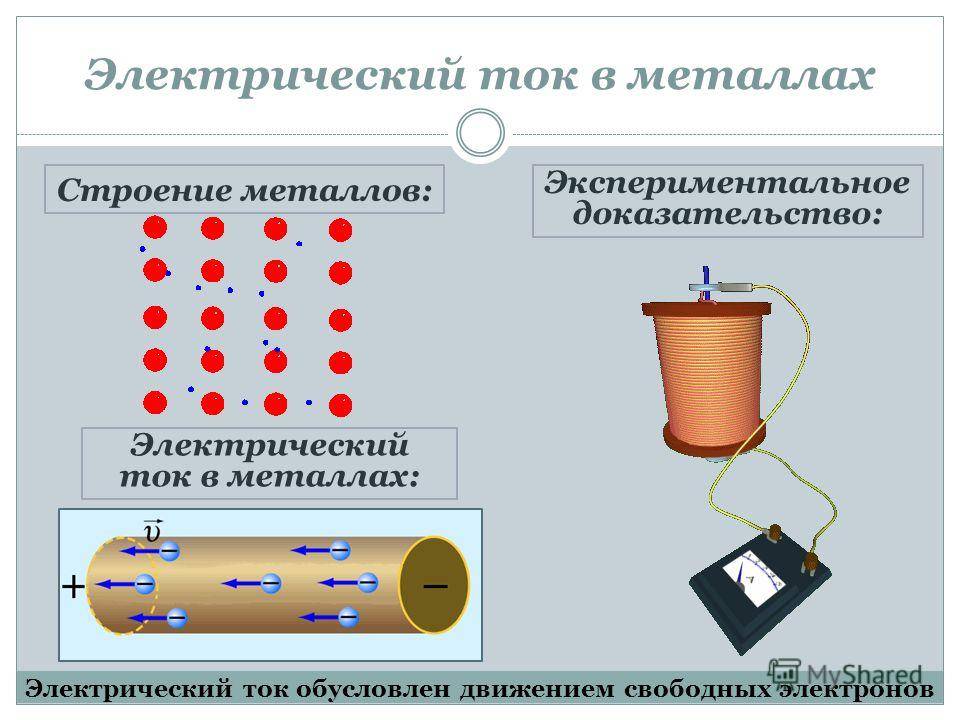
При изучении предыдущего параграфа вы узнали, что в металлах перенос заряда не сопровождается переносом вещества, а носителями свободных зарядов являются электроны. Но существует класс проводников, прохождение электрического тока в которых всегда сопровождается химическими изменениями и переносом вещества. Какова природа электрического тока в таких проводниках?
Природа электрического тока в электролитах. Из опытов следует, что растворы многих солей, кислот и щелочей, а также расплавы солей и оксидов металлов проводят электрический ток, т. е. являются проводниками. Такие проводники назвали электролитами.
Электролиты — вещества, растворы или расплавы которых проводят электрический ток.
 Рис. 200
Рис. 200
Проведём опыт. Соберём электрическую цепь, состоящую из источника тока, лампы накаливания и ванны с дистиллированной водой, в которой находятся два угольных электрода. При замыкании цепи лампа не светится, следовательно, дистиллированная вода не проводит электрический ток. Повторим опыт, добавив в дистиллированную воду сахар. Лампа не светится и в этом случае. Раствор сахара в воде также не является проводником. А теперь добавим в дистиллированную воду небольшое количество соли, например, хлорида меди(II) CuCl2. В цепи проходит электрический ток, о чём наглядно свидетельствует свечение лампы (рис. 200). Следовательно, раствор соли в воде является проводником электрического тока, т. е. при растворении хлорида меди(II) в дистиллированной воде появились свободные носители электрического заряда.
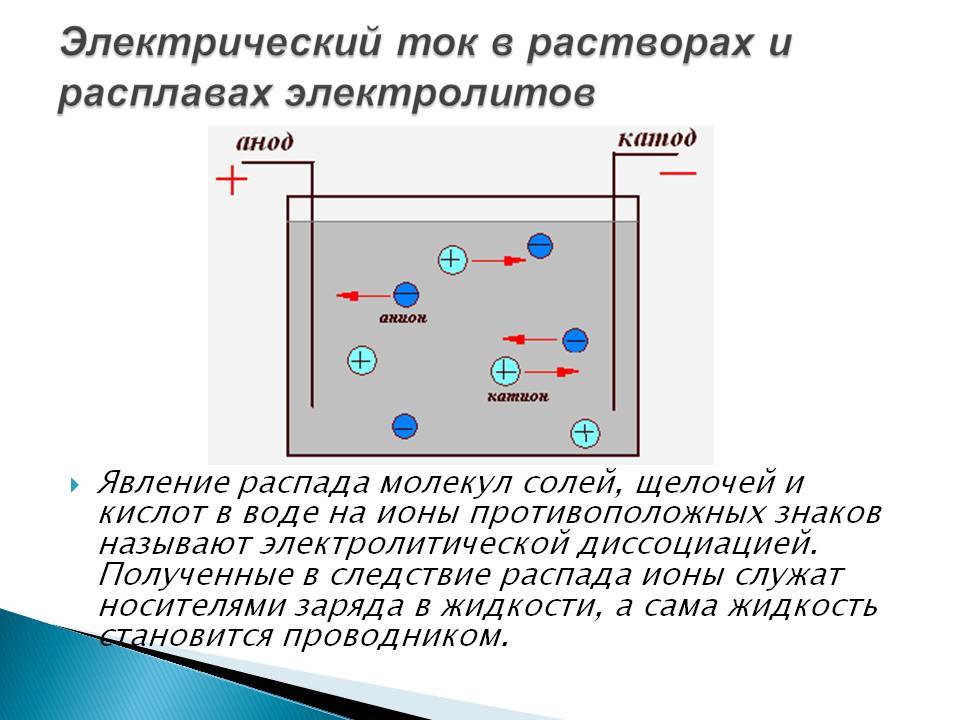
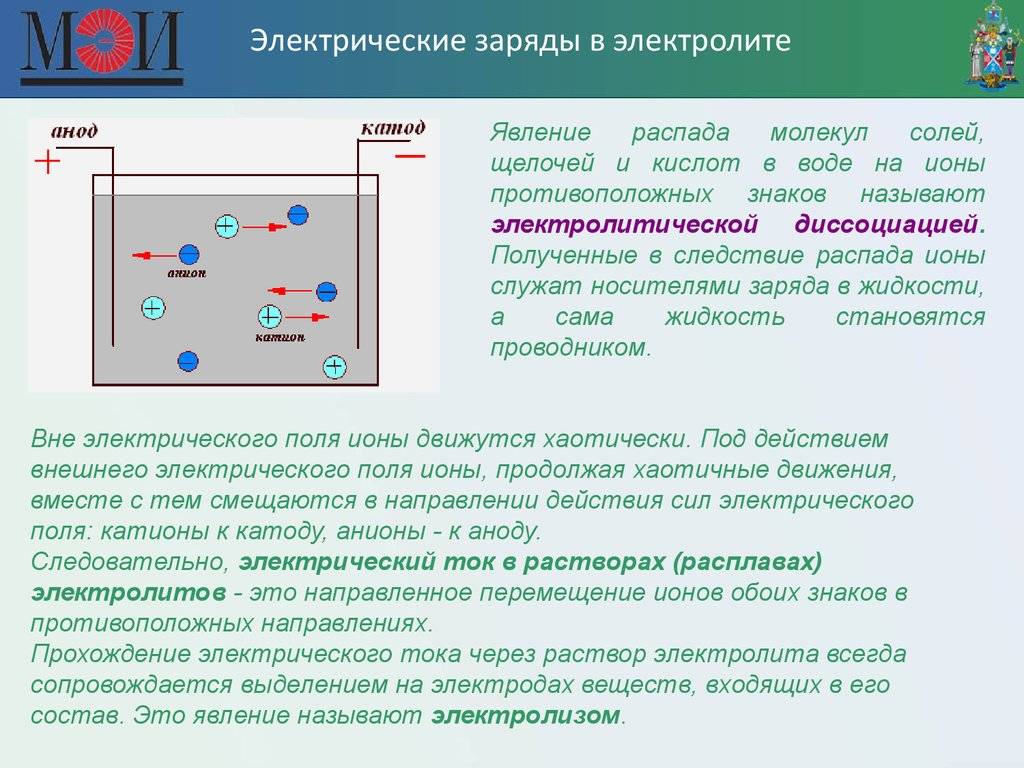
Изучая химию, вы узнали, что при растворении солей, кислот и щелочей в воде происходит электролитическая диссоциация, т. е. распад молекул электролита на ионы. В проведённом опыте хлорид меди(II) CuCl2 в водном растворе диссоциирует на положительно заряженные ионы меди Cu2+ и отрицательно заряженные ионы хлора Cl−.
 Рис. 201
Рис. 201
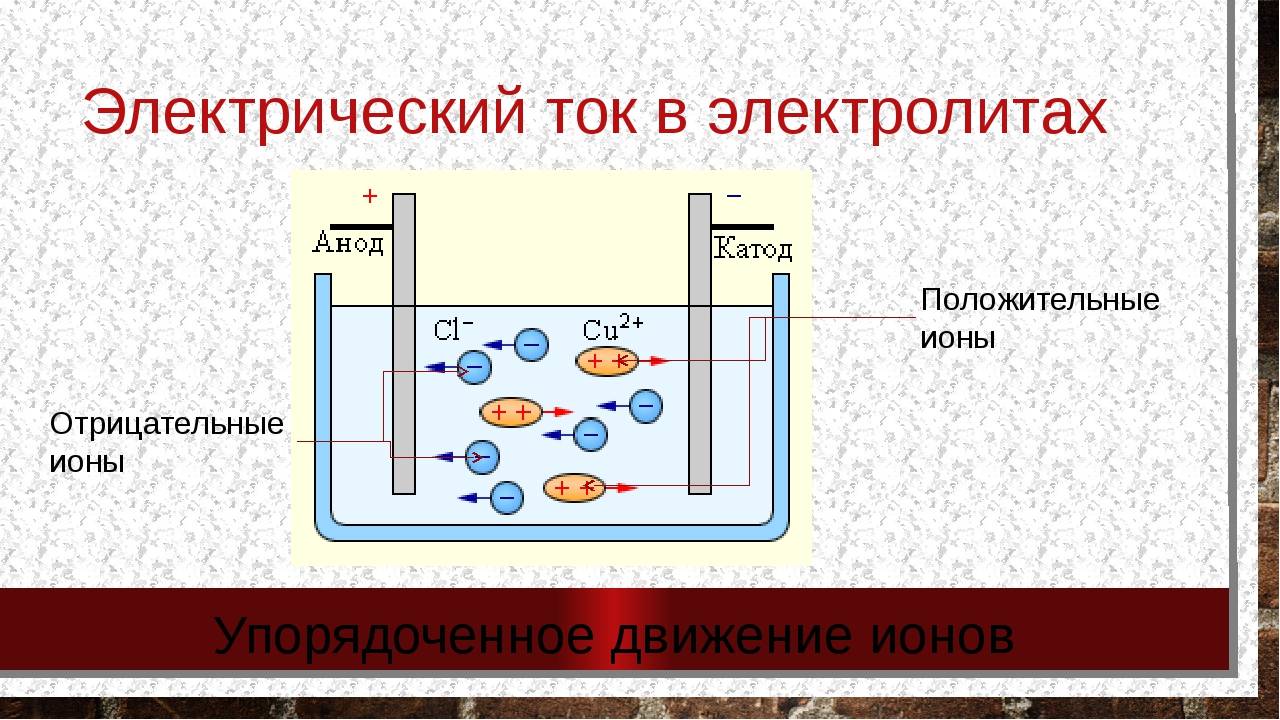
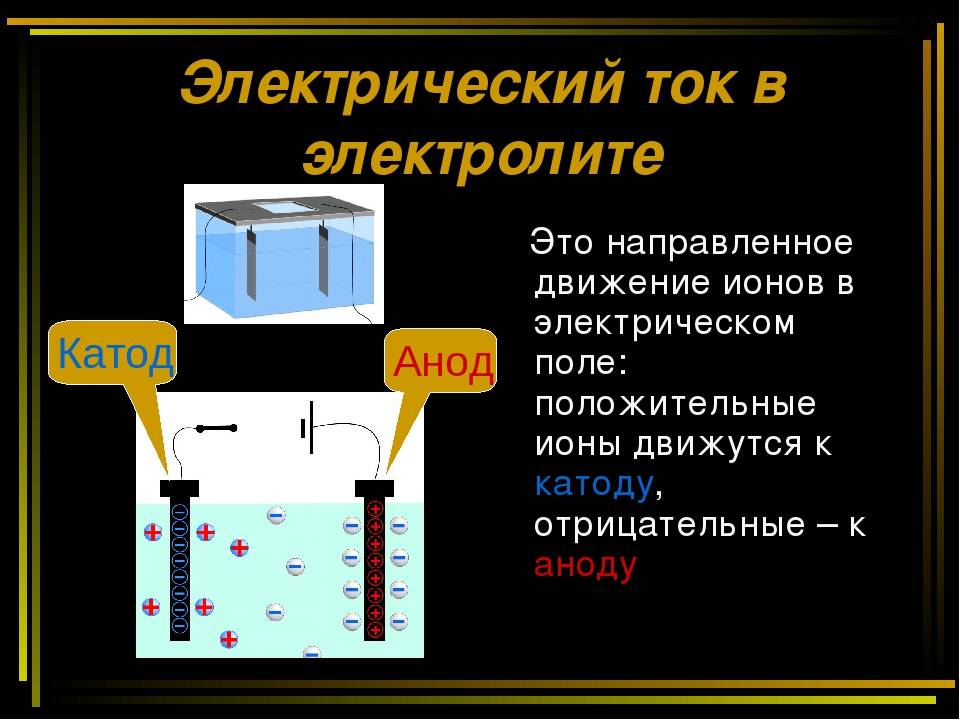
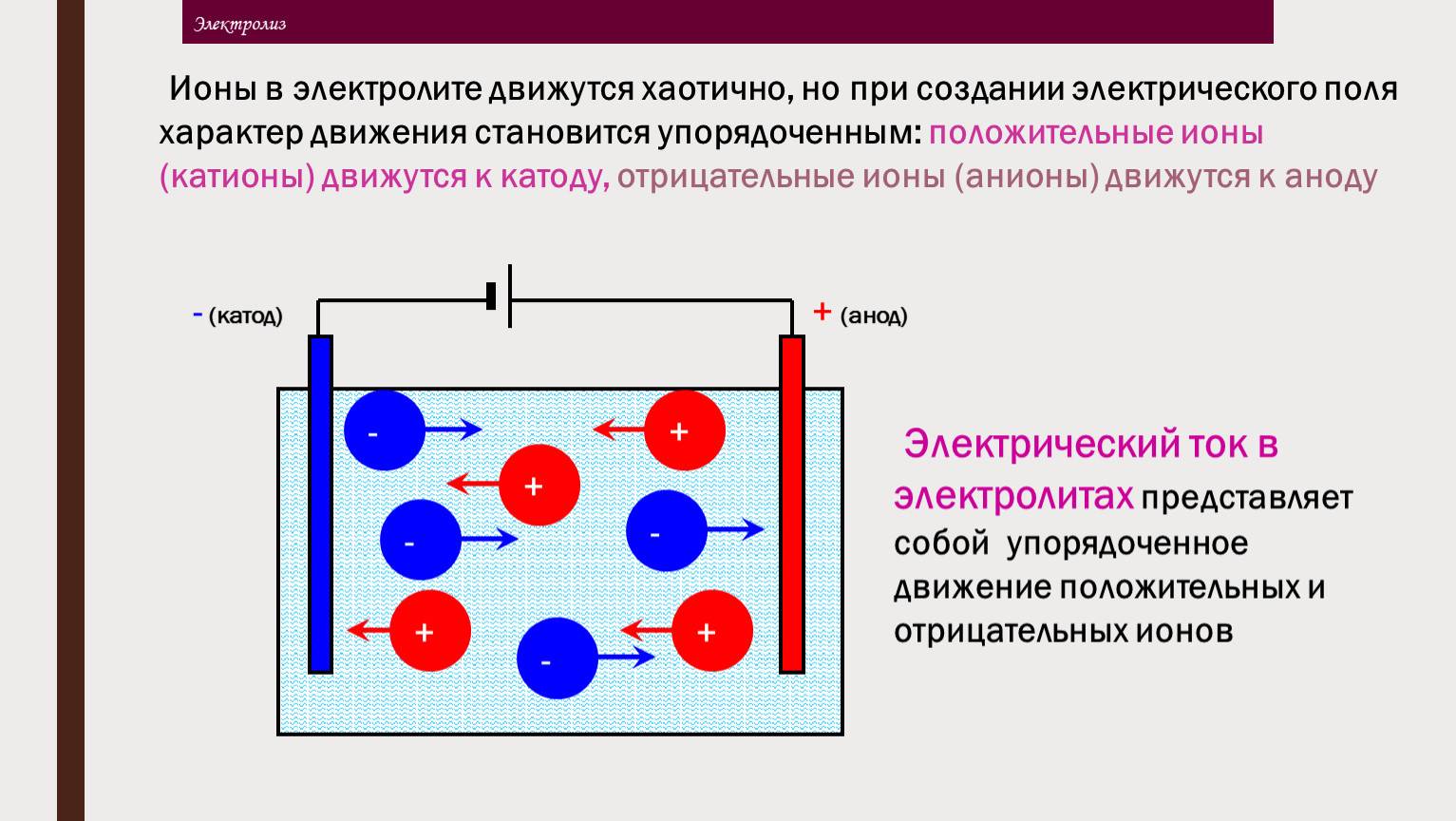
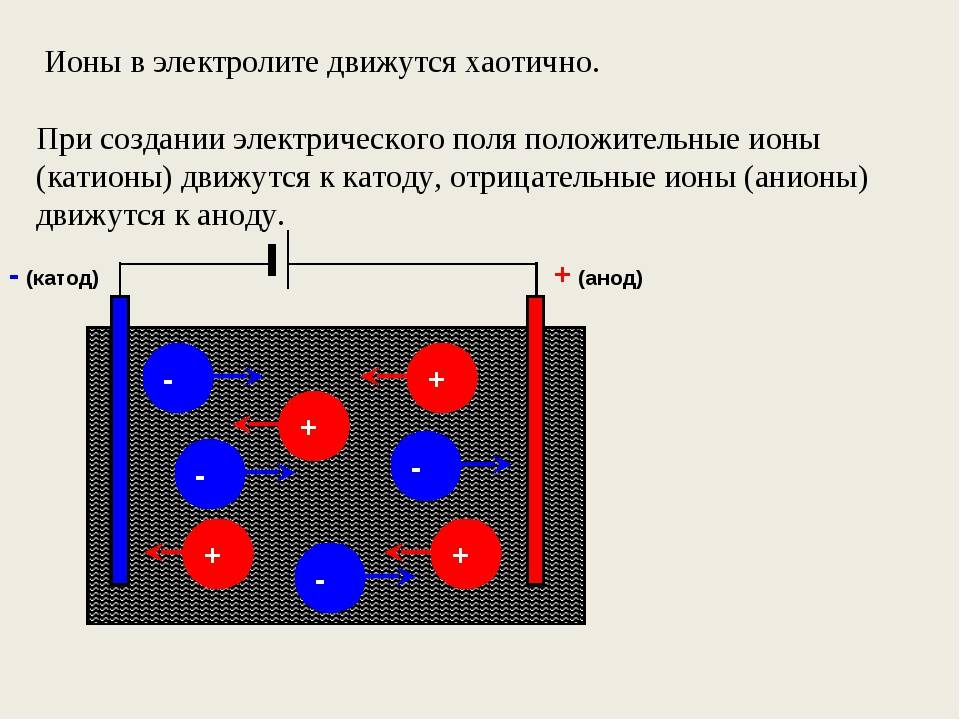
Ионы Cu2+ и Cl− в растворе при отсутствии электрического поля движутся беспорядочно. Под действием внешнего электрического поля на беспорядочное движение ионов накладывается их направленное движение (рис. 201). При этом положительно заряженные ионы Cu2+ движутся к катоду (электроду, подключённому к отрицательному полюсу источника тока), отрицательно заряженные ионы Cl− — к аноду (электроду, подключённому к положительному полюсу источника тока). На аноде будет происходить процесс окисления ионов Cl− до атомов.
Нейтральные атомы образуют молекулы хлора, который выделяется на аноде:
На катоде будет происходить процесс восстановления ионов Cu2+ до нейтральных атомов и осаждение металлической меди:
Это явление называют электролизом.
Электролиз — процесс выделения на электроде вещества, связанный с окислительно-восстановительными реакциями, протекающими при прохождении электрического тока через растворы (расплавы) электролитов.
Таким образом, свободные носители электрического заряда в электролитах — положительно и отрицательно заряженные ионы, которые образуются в результате электролитической диссоциации, а проводимость электролитов является ионной. Электролиты относят к проводникам второго рода.
От теории к практике
Почему опасно прикасаться голыми руками к неизолированным металлическим проводам, по которым проходит электрический ток?
Электрический ток в электролитах
Электролиты — жидкости, проводящие электрический ток. К ним относят растворы солей, щелочей и кислот.
Положительные ионы (катионы) движутся к катоду, а отрицательные (анионы) — к аноду.
Пример №1. Электрическая цепь, изображенная на рисунке, включает в себя сосуд со слабым раствором поваренной соли (NaCl) и опущенными в него двумя электродами. В каком направлении (вправо, влево, вверх, вниз) будут двигаться ионы натрия при замыкании ключа:
При замыкании ключа в растворе соли начнут образовываться ионы: положительные в виде Na+ и отрицательные в виде Cl–. Положительные ионы будут двигаться к отрицательному электроду (катоду), т.е. вправо.
Отсутствие электростатического поля внутри проводника
Можно рассмотреть это на примере металлической пластины. При помещении проводника в электрическое поле, в первый момент возникает электрический ток. Под действием внешнего поля электроны начинают перемещаться.
Они перераспределяются по пластине таким образом, что положительные заряды пластины оказываются со стороны отрицательных зарядов, создающих поле, и наоборот. Отрицательные заряды пластины притягиваются положительными зарядами, создающими внешнее поле.
При этом уже сами заряды пластины создают свое собственное поле, которое противоположно по направлению линиям напряженности внешнего поля и компенсирует его.
Так и выходит, что по принципу суперпозиции полей их напряженности складываются, и результирующая напряженность поля внутри проводника оказывается равной нулю. Перераспределение зарядов происходит за ничтожно короткое время, поэтому можно считать, что оно происходит мгновенно.
Выходит, что внутри тела, сделанного из проводника, электростатического поля не будет. Именно на этом свойстве металлов основано применение защиты от внешних полей.
Особо чувствительные приборы и механизмы помещают в оболочку из металла, например, в ящик или оплетают металлической сеткой, которая обладает теми же свойствами, что и цельные куски металла.
Таким образом, объекты не подвергаются внешнему воздействию вроде электризации, намагничивания и так далее.
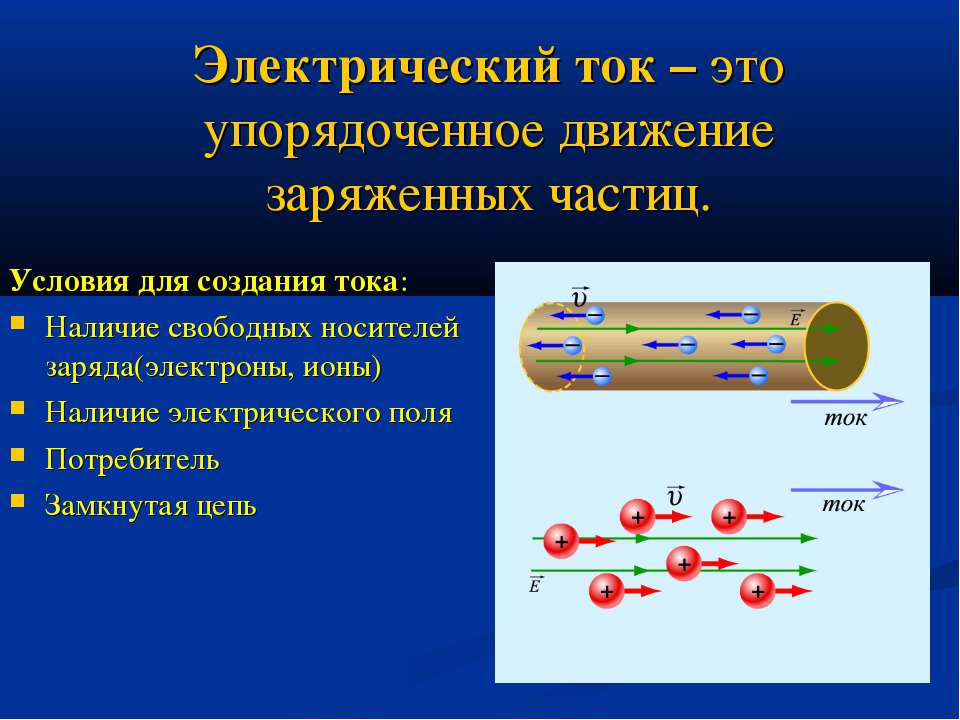
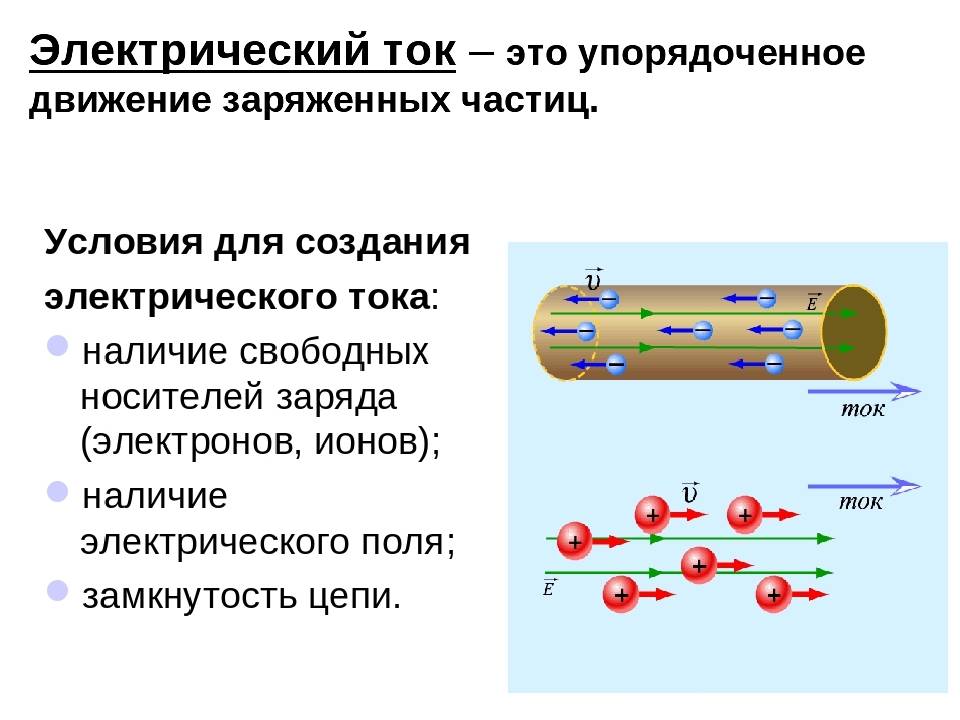
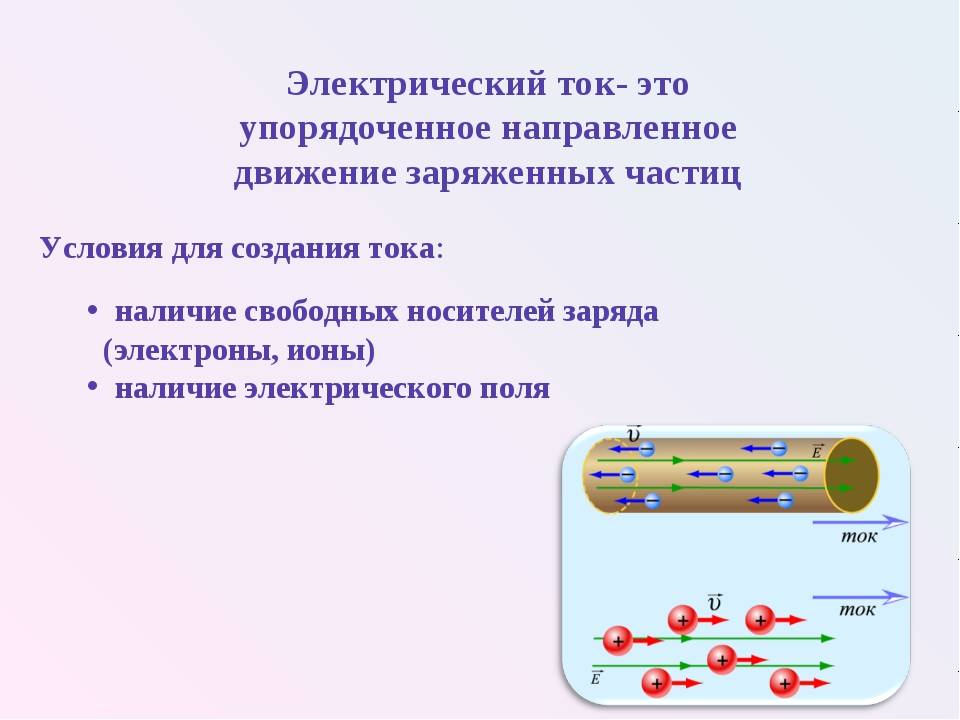
Условия для возникновения электрического тока
От какого слова образуется слово «ток». Я думаю, от слова поТОК. Поток воды, поток энергии, поток света и тд, а поток электронов в проводке называется просто «электрическим током». Значит, заставляя «течь» электроны, мы тем самым создаем электрический ток!
Теперь снова надуйте свои пухленькие щечки и пытайтесь создать внутри полости рта очень высокое давление. Что у нас произойдет? Ваши губки не выдержат и поток воздуха устремится изо рта в окружающее пространство. То есть вы создали в полости рта высокое давление, которое устремилось в область низкого давления, то есть наружу. Почти схожим образом вы создаете «ветер» из пукана, напрягая свой животик :-).
Ладно, давайте обобщим, все что мы тут пописали. ЭДС создает движение электронов по проводку. Для того, чтобы было движение, электроны должны куда-то направляться, желательно обратно к ЭДС источнику. В идеале, должно быть как-то так:

Как вы видите, труба у нас выходит из насосной станции и входит в насосную станцию. То есть контур трубы получается замкнутым. Пока работает насосная станция, у нас есть движуха воды. Как только насосная станция сломается, то движение воды прекратится
Также немаловажно чтобы труба не была тонкая в диаметре, иначе ее порвет, если насосная станция будет большой мощности
Итак, какие условия должны соблюдаться, чтобы у нас получился нескончаемый поток овец?
- у нас должно быть много свободных овец
- мы должны направить этих свободных овец в одну сторону, то есть должны их как-то заманить.
- сделать так, чтобы поток овец и гектары капусты никогда не заканчивались
Если перефразировать эти фразы на электрический ток, то получается:
- у нас в веществе должно быть множество свободных электронов
- мы должны заставить электроны двигаться в одном направлении
- сделать так, чтобы сила, толкающая электроны в одном направлении никогда не иссякала
Кто открыл, опыт Мандельштама и Папалекси
Первые опыты по изучению электрической проводимости металлов провел немецкий ученый Карл Виктор Эдуард Рикке в 1901 году. Суть эксперимента сводилась к следующему. Три отполированных цилиндра плотно прижали друг к другу, расположив в таком порядке: медь–алюминий–медь. В течение года через них пропускали ток в одном и том же направлении.
Суммарный заряд, прошедший через этот проводник за все время составил более 3,5 МКл. После завершения опыта цилиндры взвесили и выяснилось, что их массы не изменились. Это исследование стало доказательством того, что прохождение тока в металлах не связано с химическими процессами и переносом вещества, а заряд создается частицами, которые имеются у всех металлов, т.е. электронами.
Была собрана следующая установка: катушка на стержне со скользящими контактами, которые присоединены к гальванометру. Катушка вращалась с большой скоростью, затем резко останавливалась, при этом фиксировали отклонение стрелки гальванометра. В ходе эксперимента ученые установили, что электрон обладает массой. Но измерить эту массу они не смогли, опыт был только качественным.
Спустя три года физики Р. Толмен и Б. Стюарт предложили свой вариант подобного эксперимента, что позволило произвести количественные измерения. Им удалось вычислить массу электрона. Для этого они измерили заряд на выходах катушки, образующийся при торможении. После внезапной остановки катушки в цепи возникал импульс тока. Направление тока указывало на то, что он вызван движением отрицательных зарядов.
С помощью баллистического гальванометра ученые измерили суммарный заряд, проходящий по цепи, и вычислили отношение заряда одной частицы к ее массе — qm. Оно оказалось близким по значению к отношению em для электрона =1,8 ×1011 Клкг, которое на тот момент уже было известно.
Какие частицы его создают, скорость распространения тока
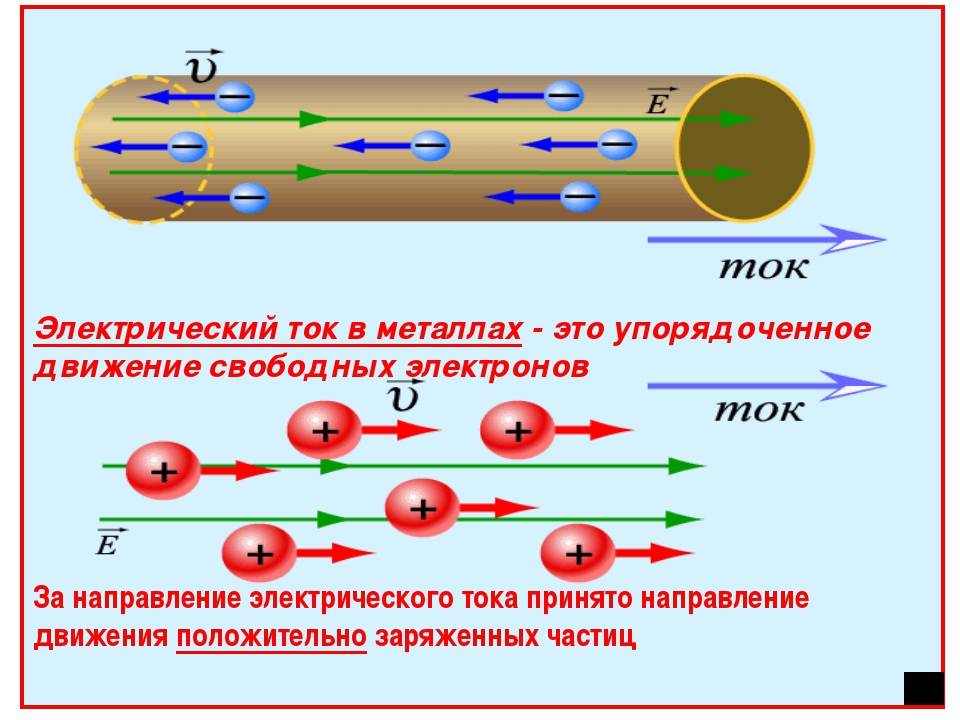
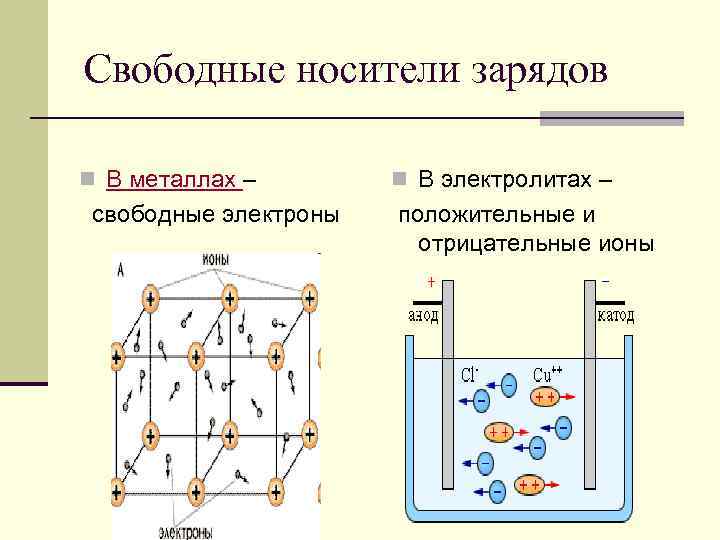
Хорошая электропроводность металлов обусловлена высокой концентрацией свободных электронов. Каждый атом металла, находящийся в узле кристаллической решетки, имеет один или несколько валентных (свободных) электронов. Валентные электроны находятся на внешней электронной оболочке и слабо связаны с ядром, поэтому атом легко с ними расстается.
Они совершают тепловое движение в различных направлениях по всему кристаллу. Положительные ионы остаются в узлах кристаллической решетки, а пространство между ними заполняется свободными электронами или так называемым электронным газом.
Если металлический проводник присоединить к источнику тока и замкнуть цепь, валентные электроны продолжают совершать хаотическое движение, но под действием возникшего внешнего электрического поля они также начинают перемещаться в одном направлении. Это упорядоченное течение электронного газа, совмещенное с тепловым движением электронов, и есть электрический ток в металле.
Скорость упорядоченного движения (дрейфовая скорость) любого электрона в проводнике не превышает 1 мм/с.
Одновременно с распространением электрического поля все электроны начинают двигаться в одном направлении по всей длине проводника.
1.15. Электрический ток в электролитах
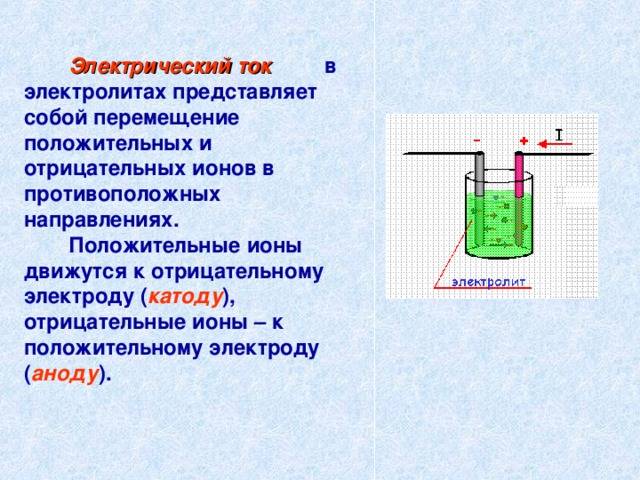
Электролитами принято называть проводящие среды, в которых протекание электрического тока сопровождается переносом вещества. Носителями свободных зарядов в электролитах являются положительно и отрицательно заряженные ионы. К электролитам относятся многие соединения металлов в расплавленном состоянии, а также некоторые твердые вещества. Однако основными представителями электролитов, широко используемыми в технике, являются водные растворы неорганических кислот, солей и оснований.
Прохождение электрического тока через электролит сопровождается выделением веществ на электродах. Это явление получило название электролиза.
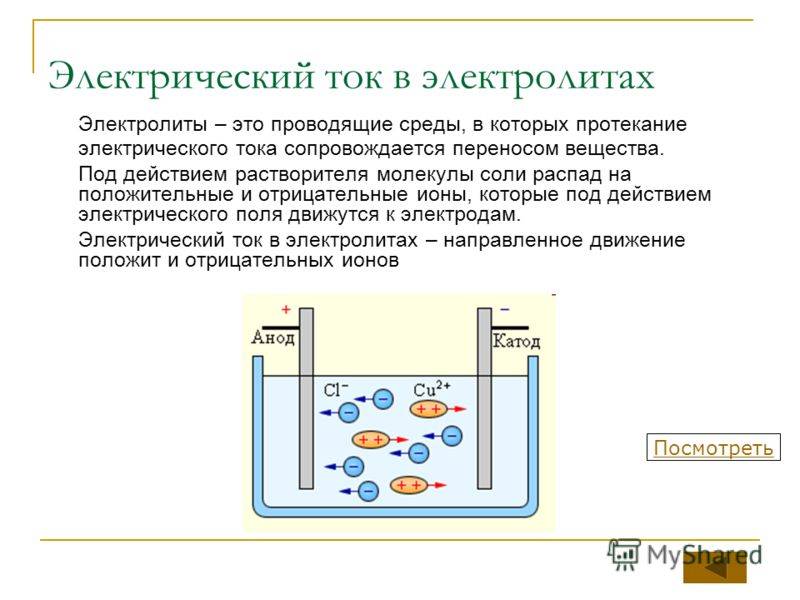
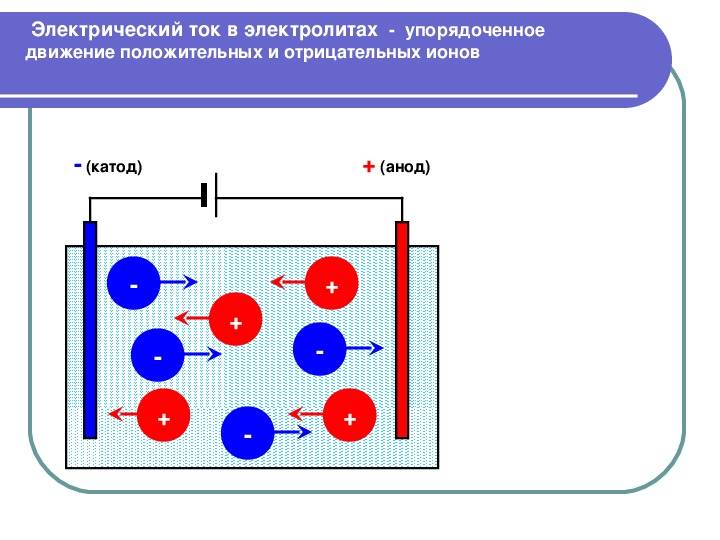
Электрический ток в электролитах представляет собой перемещение ионов обоих знаков в противоположных направлениях. Положительные ионы движутся к отрицательному электроду (катоду), отрицательные ионы – к положительному электроду (аноду). Ионы обоих знаков появляются в водных растворах солей, кислот и щелочей в результате расщепления части нейтральных молекул. Это явление называется электролитической диссоциацией. Например, хлорид меди CuCl2 диссоциирует в водном растворе на ионы меди и хлора:
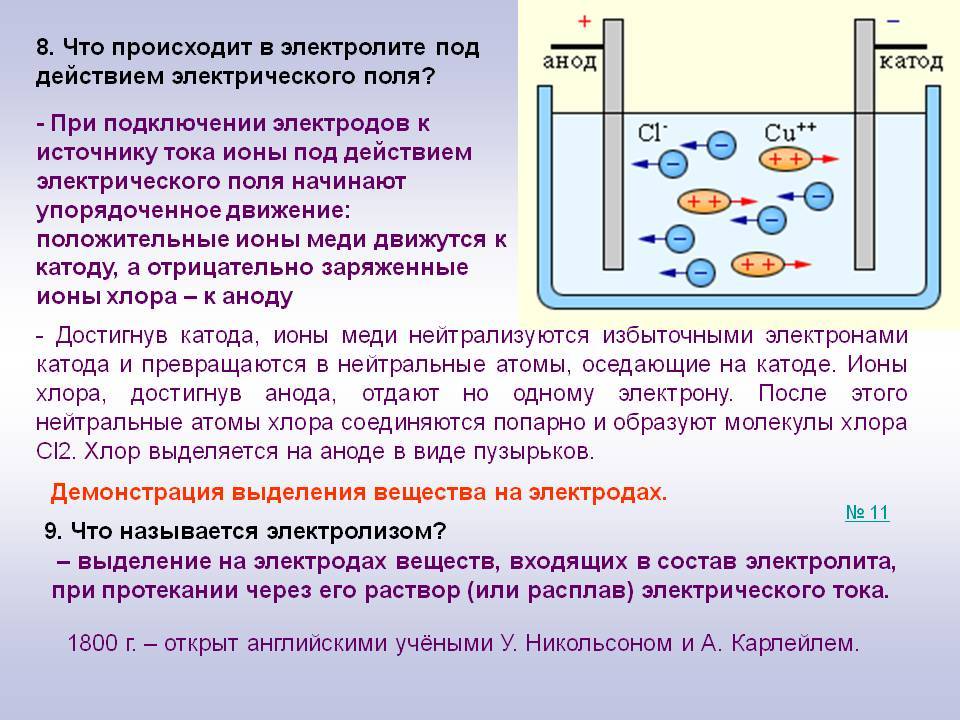
При подключении электродов к источнику тока ионы под действием электрического поля начинают упорядоченное движение: положительные ионы меди движутся к катоду, а отрицательно заряженные ионы хлора – к аноду (рис 1.15.1).
Достигнув катода, ионы меди нейтрализуются избыточными электронами катода и превращаются в нейтральные атомы, оседающие на катоде. Ионы хлора, достигнув анода, отдают по одному электрону. После этого нейтральные атомы хлора соединяются попарно и образуют молекулы хлора Cl2. Хлор выделяется на аноде в виде пузырьков.
Во многих случаях электролиз сопровождается вторичными реакциями продуктов разложения, выделяющихся на электродах, с материалом электродов или растворителей. Примером может служить электролиз водного раствора сульфата меди CuSO4 (медный купорос) в том случае, когда электроды, опущенные в электролит, изготовлены из меди.
Диссоциация молекул сульфата меди происходит по схеме
Нейтральные атомы меди отлагаются в виде твердого осадка на катоде. Таким путем можно получить химически чистую медь. Ион отдает аноду два электрона и превращается в нейтральный радикал SO4 вступает во вторичную реакцию с медным анодом:
| SO4 + Cu = CuSO4. |
Образовавшаяся молекула сульфата меди переходит в раствор.
Таким образом, при прохождении электрического тока через водный раствор сульфата меди происходит растворение медного анода и отложение меди на катоде. Концентрация раствора сульфата меди при этом не изменяется.
| Рисунок 1.15.1. Электролиз водного раствора хлорида меди |
Закон электролиза был экспериментально установлен английским физиком М. Фарадеем в 1833 году. Закон Фарадея определяет количества первичных продуктов, выделяющихся на электродах при электролизе:
Масса m вещества, выделившегося на электроде, прямо пропорциональна заряду Q, прошедшему через электролит:
| m = kQ = kIt. |
Величину k называют электрохимическим эквивалентом.
Масса выделившегося на электроде вещества равна массе всех ионов, пришедших к электроду:
Здесь m0 и q0 – масса и заряд одного иона, – число ионов, пришедших к электроду при прохождении через электролит заряда Q. Таким образом, электрохимический эквивалент k равен отношению массы m0 иона данного вещества к его заряду q0.
Так как заряд иона равен произведению валентности вещества n на элементарный заряд e (q0 = ne), то выражение для электрохимического эквивалента k можно записать в виде
Здесь NA – постоянная Авогадро, M = m0NA – молярная масса вещества, F = eNA – постоянная Фарадея.
| F = eNA = 96485 Кл / моль. |
Постоянная Фарадея численно равна заряду, который необходимо пропустить через электролит для выделения на электроде одного моля одновалентного вещества.
Закон Фарадея для электролиза приобретает вид:
Явление электролиза широко применяется в современном промышленном производстве.
Электронный ток в жидкостях кратко
«Физика — 10 класс»
Каковы носители электрического тока в вакууме?Каков характер их движения? Жидкости, как и твёрдые тела, могут быть диэлектриками, проводниками и полупроводниками. К диэлектрикам относится дистиллированная вода, к проводникам — растворы и расплавы электролитов: кислот, щелочей и солей. Жидкими полупроводниками являются расплавленный селен, расплавы сульфидов и др.
Электролитическая диссоциация.
При растворении электролитов под влиянием электрического поля полярных молекул воды происходит распад молекул электролитов на ионы.
Распад молекул на ионы под влиянием электрического поля полярных молекул воды называется электролитической диссоциацией.
Степень диссоциации — доля в растворённом веществе молекул, распавшихся на ионы.
Степень диссоциации зависит от температуры, концентрации раствора и электрических свойств растворителя.
С увеличением температуры степень диссоциации возрастает и, следовательно, увеличивается концентрация положительно и отрицательно заряженных ионов.
Ионы разных знаков при встрече могут снова объединиться в нейтральные молекулы.
При неизменных условиях в растворе устанавливается динамическое равновесие, при котором число молекул, распадающихся за секунду на ионы, равно числу пар ионов, которые за то же время вновь объединяются в нейтральные молекулы.
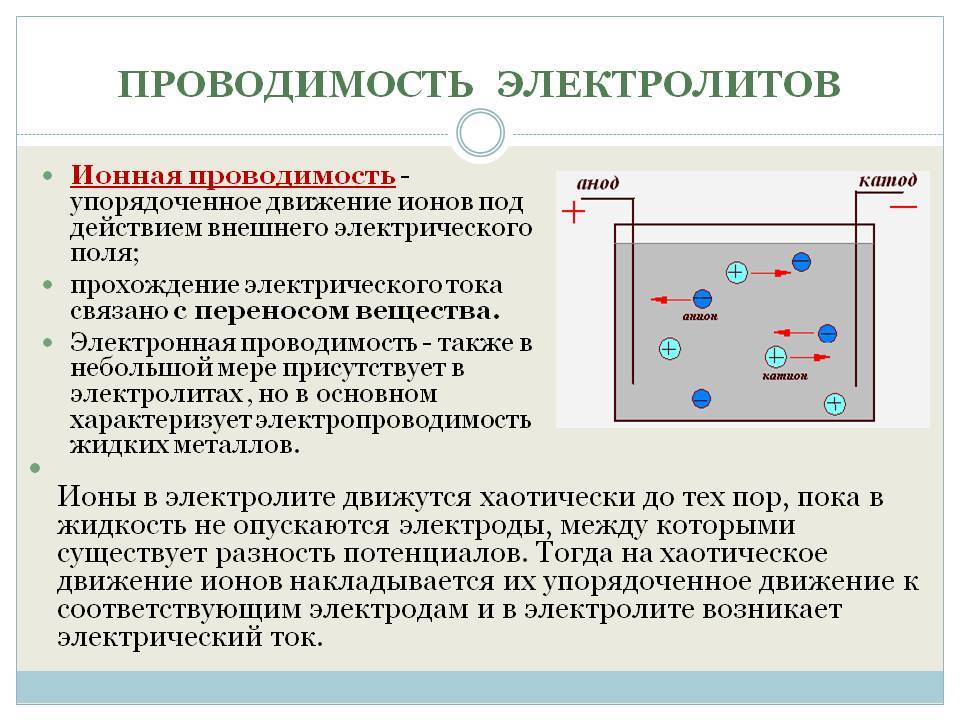
Ионная проводимость.
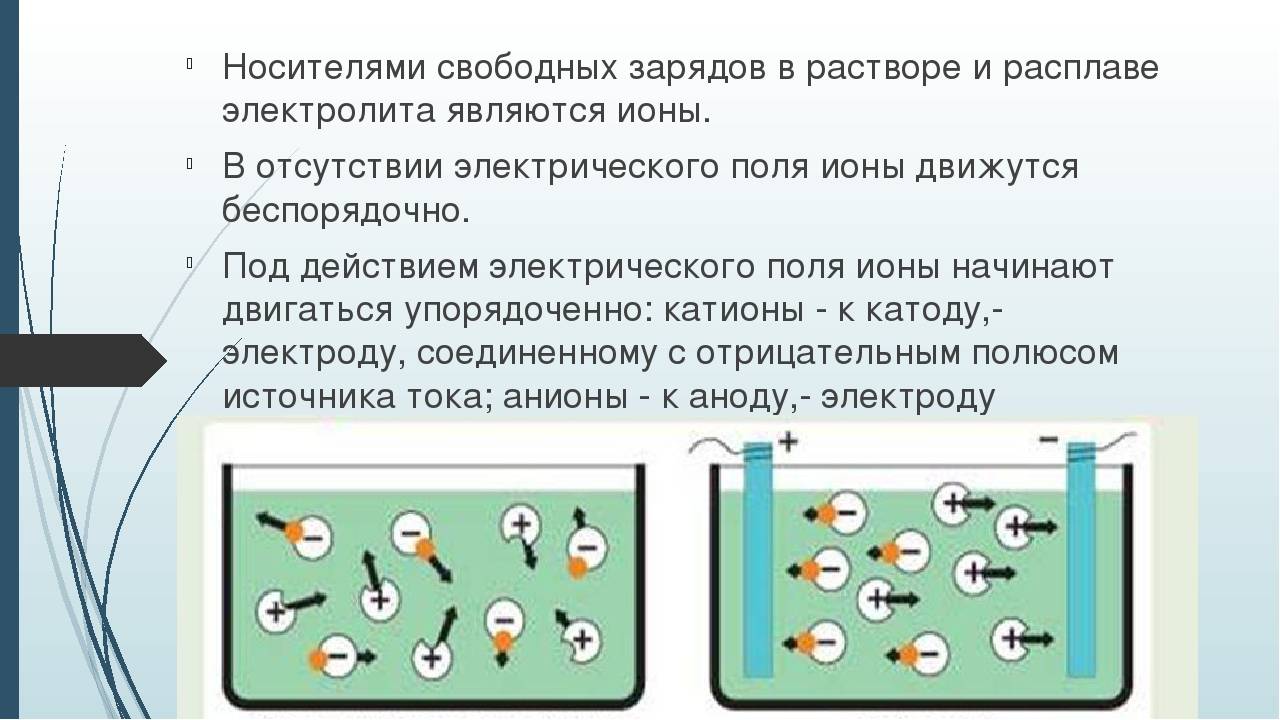
Носителями заряда в водных растворах или расплавах электролитов являются положительно и отрицательно заряженные ионы.
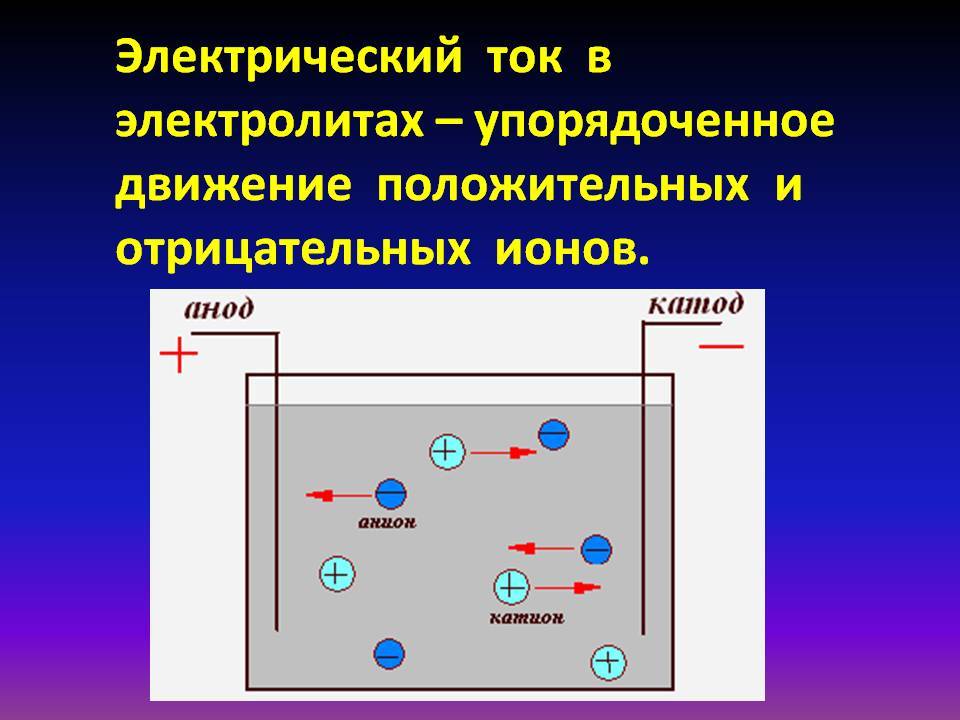
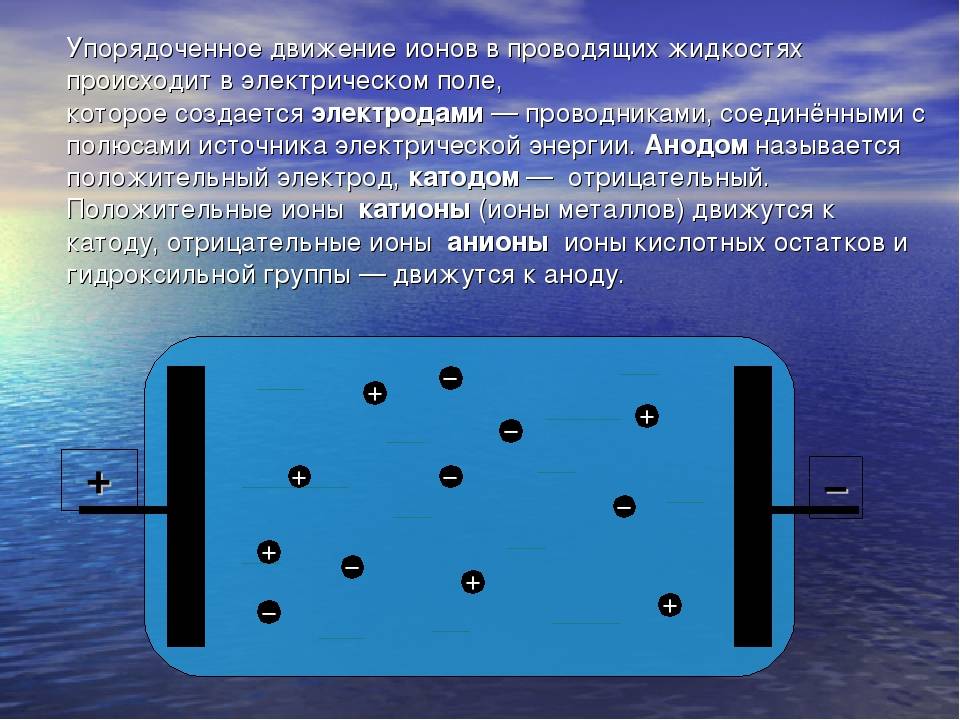
Если сосуд с раствором электролита включить в электрическую цепь, то отрицательные ионы начнут двигаться к положительному электроду — аноду, а положительные — к отрицательному — катоду. В результате по цепи пойдёт электрический ток.
Проводимость водных растворов или расплавов электролитов, которая осуществляется ионами, называют ионной проводимостью.
Жидкости могут обладать и электронной проводимостью. Такой проводимостью обладают, например, жидкие металлы.
Электролиз. При ионной проводимости прохождение тока связано с переносом вещества. На электродах происходит выделение веществ, входящих в состав электролитов. На аноде отрицательно заряженные ионы отдают свои лишние электроны (в химии это называется окислительной реакцией), а на катоде положительные ионы получают недостающие электроны (восстановительная реакция).
Жидкости могут обладать и электронной проводимостью. Такой проводимостью обладают, например, жидкие металлы.
Процесс выделения на электроде вещества, связанный с окислительновосстановительными реакциями, называют электролизом.
От чего зависит масса вещества, выделяющегося за определённое время? Очевидно, что масса m выделившегося вещества равна произведению массы m0i одного иона на число Ni ионов, достигших электрода за время Δt:
Масса иона m0i равна:
где М — молярная (или атомная) масса вещества, a NA — постоянная Авогадро, т. е. число ионов в одном моле.
Число ионов, достигших электрода, равно:
где Δq = IΔt — заряд, прошедший через электролит за время Δt; q0i — заряд иона, который определяется валентностью n атома: q0i = пе (е — элементарный заряд). При диссоциации молекул, например КВr, состоящих из одновалентных атомов (n = 1), возникают ионы К + и Вr — . Диссоциация молекул медного купороса ведёт к появлению двухзарядных ионов Си 2+ и SO 2- 4 (n = 2). Подставляя в формулу (16.3) выражения (16.4) и (16.5) и учитывая, что Δq = IΔt, a q0i = nе, получаем
Закон Фарадея.
Обозначим через k коэффициент пропорциональности между массой m вещества и зарядом Δq = IΔt, прошедшим через электролит:
где F = eNA = 9,65 • 10 4 Кл/моль — постоянная Фарадея
Коэффициент k зависит от природы вещества (значений М и n). Согласно формуле (16.6) имеем
Закон электролиза Фарадея:
Масса вещества, выделившегося на электроде за время Δt. при прохождении электрического тока, пропорциональна силе тока и времени.
Это утверждение, полученное теоретически, впервые было установлено экспериментально Фарадеем.
Величину k в формуле (16.8) называют электрохимическим эквивалентом данного вещества и выражают в килограммах на кулон
(кг/Кл).
Из формулы (16.8) видно, что коэффициент к численно равен массе вещества, выделившегося на электродах, при переносе ионами заряда, равного 1 Кл.
Электрохимический эквивалент имеет простой физический смысл. Так как M/NA = m0i и еn = q0i, то согласно формуле (16.7) k = rn0i/q0i, т. е. k — отношение массы иона к его заряду.
Применение свойств электрического тока в металлах
Имеет отношение к следующим отраслям:
- Передача электроэнергии от источника к потребителям.
- Электродвигатели.
- Нагревательные приборы всех типов, предназначенных для промышленности и домашнего использования: спирали для ламп освещения, нагревательные спирали тэнов (обогреватели, чайники и т.д.).
- Получение сильных магнитных полей (МРТ, электромагниты со сверхпроводящей обмоткой в ускорителях для ракет и генераторов).
- Электроизмерительные приборы: амперметры, вольтметры, электрические счетчики и др.
- В металлургии:
- гальваностегия — электрохимический процесс покрытия одних металлов другими, более устойчивыми к коррозии: золочение, серебрение, никелирование и т. д. Используется также для придания изделиям декоративного вида;
- гальванопластика — получение металлических копий с рельефов. Гипсовый оттиск рельефа покрывают слоем графита и погружают в электролит — раствор соли металла, который осаждается на оттиске, как на катоде. После удаления гипса получается металлическая копия рельефа;
- электролитическое рафинирование позволяет очищать цветные металлы от примесей.
Электрическая диссоциация
Это основополагающий процесс для появления электротока в растворах, поэтому его необходимо рассмотреть более подробно. Все ионы, образующиеся при распаде молекул, можно разделить на 2 типа:

- Анионы. Имеют отрицательный заряд.
- Катионы. Обладают положительным зарядом.
Большинство свойств воды обусловлено полярностью молекул вещества. Говоря иначе, с точки зрения электротехники они являются диполями. Здесь следует вспомнить определение диполи — это система двух частиц, расположенных близко друг к другу. При этом их заряды противоположны по знаку, но одинаковы по модулю. Свойство полярности H2O объясняется геометрическим строением молекул вещества:
- угол между центральными линиями атомов равен примерно 104,5 градуса;
- электронны смещены в направлении кислорода.

Чтобы установить, какова природа процесса распада молекул на ионы, следует рассмотреть раствор поваренной соли. На внешней орбите атома натрия расположен лишь 1 электрон. Его связь с атомом слаба, поэтому он способен быстро уйти со своего места. У атома хлора на внешней орбите находится уже 7 электронов и до комплекта не хватает одной частицы. Благодаря этому при образовании кристалла NaCl внешний электрон натрия присоединяется к атому хлора. В итоге образуется диполь.
Взаимодействие двух видов диполей и способствуют активизации процесса растворения. Если в раствор электролита поместить 2 электрода — катод (отрицательный) и анод (положительный), то свободные ионы устремятся к ним. При этом направление их движения протекает по конкретным правилам:
- катионы направятся к катоду;
- анионы начинают двигаться в направлении анода.
Электрическая диссоциация
Это основополагающий процесс для появления электротока в растворах, поэтому его необходимо рассмотреть более подробно. Все ионы, образующиеся при распаде молекул, можно разделить на 2 типа:

- Анионы. Имеют отрицательный заряд.
- Катионы. Обладают положительным зарядом.
Большинство свойств воды обусловлено полярностью молекул вещества. Говоря иначе, с точки зрения электротехники они являются диполями. Здесь следует вспомнить определение диполи — это система двух частиц, расположенных близко друг к другу. При этом их заряды противоположны по знаку, но одинаковы по модулю. Свойство полярности H2O объясняется геометрическим строением молекул вещества:
- угол между центральными линиями атомов равен примерно 104,5 градуса;
- электронны смещены в направлении кислорода.
Чтобы установить, какова природа процесса распада молекул на ионы, следует рассмотреть раствор поваренной соли. На внешней орбите атома натрия расположен лишь 1 электрон. Его связь с атомом слаба, поэтому он способен быстро уйти со своего места. У атома хлора на внешней орбите находится уже 7 электронов и до комплекта не хватает одной частицы. Благодаря этому при образовании кристалла NaCl внешний электрон натрия присоединяется к атому хлора. В итоге образуется диполь.
Взаимодействие двух видов диполей и способствуют активизации процесса растворения. Если в раствор электролита поместить 2 электрода — катод (отрицательный) и анод (положительный), то свободные ионы устремятся к ним. При этом направление их движения протекает по конкретным правилам:
- катионы направятся к катоду;
- анионы начинают двигаться в направлении анода.
Электролитическая диссоциация
Если вещество, молекулы которого образованы ионной связью расплавить, то сперва молекулы за счет температуры удаляются друг от друга все дальше, а потом наступает определенный момент, когда и ионы, образующие молекулы, тоже удаляются настолько далеко друг от друга, что им становится возможным образовывать ионные связи с другими ионами. Таким образом, в расплаве вещества за счет температуры появляются подвижные заряженные частицы, способные двигаться под действием внешнего электрического поля.
Воздействие температуры можно заменить воздействием растворителя. Если молекулы растворителя являются диполем (например, обычная вода), то эти молекулы могут взаимодействовать с ионами кристаллической решетки растворяемого вещества, унося их в раствор. В растворе появляются заряженные частицы, способные двигаться под действием электрического поля. Происходит это, как правило, при более низких температурах. Например, если расплав поваренной соли требует температуры более 800⁰C, то растворение соли происходит при комнатной температуре.
Распад вещества на ионы с образованием проводящего электролита под действием температуры или растворителя называется электролитической диссоциацией.
Рис. 3. Ионная электролитическая диссоциация.
Таким образом, жидкость может проводить электрический ток, если она, либо сама состоит из ионов, либо является раствором вещества с ионной связью.
Что мы узнали?
Электрический ток в жидкостях может существовать, если жидкость содержит свободные заряженные частицы – ионы. Такие частицы могут существовать, либо если молекулы жидкости состоят из ионов, либо если в жидкости растворено вещество с ионной связью (например, расплав или раствор поваренной соли). Жидкость, не содержащая ионов (например, химически чистая вода) электрический ток не проводит.
/10
Вопрос 1 из 10
Почему металлы хорошие проводники
Ведь все заряженные частицы являются частью атомов вещества. Дело в том, что в металлах в процессе образования кристаллической решетки атомы вещества сильно взаимодействуют друг с другом, следствием чего является потеря электронами связи с ядрами своих атомов.
Они остаются связанными только с самой формой вещества, не имея возможности покинуть его границы, но свободно перемещающимися внутри кристаллической решетки в любых направлениях.
Такая особенность металлов дает возможность существования электрического тока внутри проводника, а также обусловливает еще одно интересное свойство металлов, на котором стоит остановиться подробнее.
При наличии внешнего электростатического поля напряженность поля внутри проводника равна нулю. Это происходит вследствие свойства электростатической индукции.
Передача электричества
Электрический ток – это упорядоченное движение заряженных частиц. Носителями заряда электрического тока в электролитах являются ионы. Они образуются в результате распада (электролитической диссоциации) молекул вещества под действием молекул воды в растворе или при нагревании и образовании расплава.
Расщепление молекул происходит за счёт разрыва полярных ковалентных или ионных связей. Интенсивность диссоциации зависит от температуры и концентрации раствора. Также на степень диссоциации влияет природа электролита. В связи с этим выделяют:
- слабые электролиты, распадающиеся частично или не распадающиеся вообще;
- сильные электролиты, быстро распадающиеся на ионы.
К слабым электролитам относится большинство органических веществ, слабые кислоты, плохо растворимые соли и нерастворимые основания. Сильные кислоты, щёлочи, соли относятся к сильным электролитам.
Рис. 1. Процесс электролитической диссоциации.
Образованные в результате диссоциации ионы делятся на два типа:
- катионы – положительно заряженные частицы;
- анионы – отрицательно заряженные частицы.
Проводником электрического тока в электролитах является электрод. Он может быть анодом или катодом. Анод присоединён к положительному полюсу источника тока, катод – к отрицательному. Анод окисляет вещества, находящиеся в электролите, катод – восстанавливает.
Рис. 2. Электроды.
Если в раствор электролита поместить два электрода – катод и анод – и включить электрический ток, то ионы начнут двигаться под действием электрического поля. Катионы устремятся к катоду, анионы – к аноду. Достигнув электродов, ионы нейтрализуются, превращаются в нейтральные атомы и оседают.
Процесс разложения вещества на составные части, которые оседают на электродах, называется электролизом.
Резюме
- В проводящих материалах внешние электроны в каждом атоме могут легко приходить или уходить и называются свободными электронами.
- В диэлектрических (изолирующих) материалах внешние электроны перемещаются не так свободно.
- Все металлы проводят электрический ток.
- Динамическое электричество, или электрический ток, – это равномерное движение электронов по проводнику.
- Статическое электричество – это неподвижный (если он находится на диэлектрике), накопленный заряд, образованный избытком или недостатком электронов в объекте. Обычно он образуется путем разделения заряда путем контакта и разделения разнородных материалов.
- Чтобы электроны могли непрерывно (бесконечно) течь через проводник, должен существовать полный, непрерывный путь, по которому они могут двигаться как внутрь, так и из этого проводника.